


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:

| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
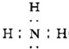
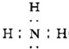
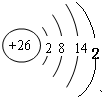

| 2b |
| a |
| 2b |
| a |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
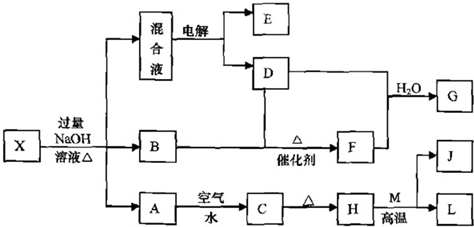
(分)有一化合物X,可发生如下的转化关系(部分反应物、生成物从略)。其中B、D、E、F均为无色气体,W、K为常见的金属单质,C为难溶于水的红褐色固体。在混合液中加入BaCl2溶液可生成不溶于稀盐酸的白色沉淀,H和W反应可放出大量的热。
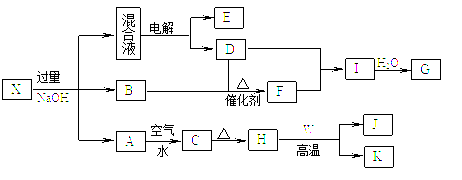 |
⑴X中滴入少量NaOH溶液的离子方程式为_______________________。
⑵B和D反应生成F的化学方程式为_____________________________。
⑶I转化为G的反应中,当有2 molG生成时,转移的电子数为_______。
⑷引发H和W反应的操作是____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com