
| 物质 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
| 溶解度 (g/100g水) | 0 | 28 | 35.7 | 4.7 | 163 |
| 40 | 40.1 | 36.4 | 26.3 | 215 | |
| 80 | 51.3 | 38 | 73 | 376 | |
分析 (1)反应中Fe、Cr元素化合价升高,结合元素守恒可知缺陷物质为氧气,Fe元素化合价由+2价升高为+3价,Cr元素化合价由+3价升高为+6价,总升高+7价,O元素化合价由0价降低为-2价,共降低4价,化合价升降最小公倍数为28,故FeO•Cr2O3的系数为4,氧气系数为7,再根据原子守恒配平;
(2)焙烧时MgO未反应,焙烧后的固体加水浸取,分离得到固体A为Fe2O3、MgO;
(3)根据平衡移动原理分析;
(4)①温度对氯化钠的溶解度影响小,但对重铬酸钾的溶解度影响较大,低温下得到溶解度更小的物质;
②加入KCl固体后,利用溶解度不同,温度对溶解度影响,经过加热浓缩、冷却结晶、过滤、洗涤、干燥可以得到K2Cr2O7晶体;
(5)固体B中主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,为精确分析B中氢氧化铝含量,先利用氢氧化铝的两性,用过量的氢氧化钠溶液溶解氢氧化铝,过滤除去不溶物,向滤液中通入二氧化碳重新生成氢氧化铝沉淀,灼烧得到氧化铝固体,根据铝元素守恒计算样品中氢氧化铝的质量,进而计算其质量分数.
解答 解:(1)反应中Fe、Cr元素化合价升高,结合元素守恒可知缺陷物质为氧气,Fe元素化合价由+2价升高为+3价,Cr元素化合价由+3价升高为+6价,总升高+7价,O元素化合价由0价降低为-2价,共降低4价,化合价升降最小公倍数为28,故FeO•Cr2O3的系数为4,氧气系数为7,再根据原子守恒配平后方程式为:4FeO•Cr2O3+8Na2CO3+7O2$\frac{\underline{\;高温\;}}{\;}$8Na2CrO4+2Fe2O3+8CO2,
故答案为:4;8;7O2;8;2;8;
(2)焙烧时MgO未反应,焙烧后的固体加水浸取,分离得到固体A为Fe2O3、MgO,
故答案为:Fe2O3、MgO;
(3)由于存在反应平衡Cr2O72-+H2O?2CrO42-+2H+,加入酸,氢离子浓度增大,平衡左移,作用是使CrO42-转化为Cr2O72-,
故答案为:使CrO42-转化为Cr2O72-;
(4)①温度对氯化钠的溶解度影响小,但对重铬酸钾的溶解度影响较大,低温下四种物质中K2Cr2O7的溶解度最小,利用复分解反应在低温下可以得到重铬酸钾,
故答案为:温度对氯化钠的溶解度影响小,但对重铬酸钾的溶解度影响较大,低温下四种物质中K2Cr2O7的溶解度最小,利用复分解反应在低温下可以得到重铬酸钾;
②加入KCl固体后,利用溶解度不同,温度对溶解度影响,再经过加热浓缩、冷却结晶、过滤、洗涤、干燥可以得到K2Cr2O7晶体,
故答案为:加热浓缩、冷却结晶;
(5)固体B中主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,为精确分析B中氢氧化铝含量,先利用氢氧化铝的两性,用过量的氢氧化钠溶液溶解氢氧化铝,过滤除去不溶物,向滤液中通入二氧化碳重新生成氢氧化铝沉淀,灼烧得到氧化铝固体,
根据Al元素守恒,样品中氢氧化铝的质量分数=$\frac{\frac{mg}{102g/mol}×2×78g/mol}{ng}$=$\frac{26m}{17n}$,
故答案为:NaOH溶液;$\frac{26m}{17n}$.
点评 本题考查物质制备、物质含量测定、物质的分离提纯、氧化还原反应、平衡移动原理等,注意对溶解度数据的分析运用,理解复分解反应本质,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | PH=1的稀硫酸中含有的H+数为0.1NA | |
| B. | 1mol苯分子中含有的碳碳双键数为3NA | |
| C. | 18gH2O中含有的质子数为10NA | |
| D. | 50mL12mol•L-1的盐酸与足量的MnO2共热,生成的Cl2分子数为0.15NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石墨比金刚石稳定 | |
| B. | 等质量的石墨比金刚石能量高 | |
| C. | 发生了物理变化 | |
| D. | 金刚石转化为石墨没有化学键的断裂与生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
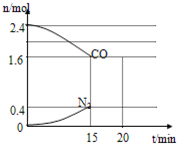 CO和NO是汽车尾气的主要污染物.消除汽车尾气的反应式之一为:2NO(g)+2CO(g)?N2(g)+2CO2(g).请回答下列问题:
CO和NO是汽车尾气的主要污染物.消除汽车尾气的反应式之一为:2NO(g)+2CO(g)?N2(g)+2CO2(g).请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按照规定对生活废弃物进行分类放置,实现资源再利用 | |
| B. | 防治环境污染、开发智能软件、合成新材料等,都属于化学研究的领域 | |
| C. | 利用人工光合成反应,将二氧化碳转化为碳氢化合物作燃料,属于低碳技术 | |
| D. | 液晶态介于晶体状态和液态之间,液晶具有有一定程度的晶体的有序性和液体的流动性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质、淀粉和油脂都属于高分子化合物 | |
| B. | 人造纤维.合成纤维.碳纤维.光导纤维主要成分都是纤维素 | |
| C. | 误食重金属盐类时,可以喝大量牛奶、蛋清或豆浆解毒 | |
| D. | 福尔马林主要成分是甲酸,由于可使蛋白质变性,可用于保存动物标本 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com