
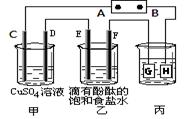
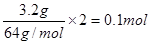 ,所以乙中生成的氢氧化钠是0.1mol,浓度是0.1mol/L,则pH=13。
,所以乙中生成的氢氧化钠是0.1mol,浓度是0.1mol/L,则pH=13。

科目:高中化学 来源:不详 题型:单选题
| A.CuCl2(CuSO4) | B.NaOH(H2O) | C.AgNO3 (AgNO3) | D.CuSO4(Cu2O) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.10m n | B.10m | C.10n | D.40mn |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
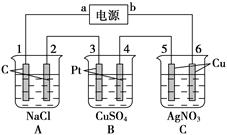
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Mg(NO3)2 | B.Al(NO3)3 | C.NH4NO3 | D.Cu(NO3)2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解饱和的食盐水,阳极产物是氢氧化钠和氯气 |
| B.电解饱和的氯化钠溶液,在阴极析出钠 |
| C.电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为2:1 |
| D.电解熔融的氯化钠,在阴极上和阳极上析出产物的物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 3H2↑+FeO42-。下列说法正确的是
3H2↑+FeO42-。下列说法正确的是| A.铁为阳极,H2SO4为电解液 |
| B.铁为阴极,浓NaOH为电解液 |
| C.阳极发生的电极反应为:Fe+80H--6e-=====4H20+Fe042- |
| D.铁失去3mol电子可以在阴极得到33.6L氢气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com