
【题目】填空:
(1)同温同压下,同体积的甲烷和二氧化碳物质的量之比为____,质量比为____;
(2)在标准状况下,4 g H2,11.2 L O2,1 mol H2O中,所含分子数最多的是______,体积最小的是________;
(3)硫酸钾和硫酸铝的混合溶液中,已知其中Al3+的浓度为0.4 mol/L,SO42-的浓度为0.7 mol/L,则K+的浓度为________mol/L
【答案】1:1 4:11 H2 H2O 0.2
【解析】
(1)由阿伏加德罗定律可知,同温同压下,同体积的甲烷和二氧化碳分子数目相同,物质的量相同,由m=nM计算质量比;
(2)物质的物质的量越大,所含分子数越大;标准状况下,水为固态,1mol水的体积小于气体体积;
(3)由溶液中电荷守恒关系计算可得。
(1)由阿伏加德罗定律可知,同温同压下,同体积的甲烷和二氧化碳分子数目相同,物质的量相同,则物质的量之比为1:1,甲烷的相对分子质量为16,二氧化碳的相对分子质量为44,则质量之比为16:44=4:11,故答案为:1:1; 4:11;
(2)在标准状况下,4 g H2的物质的量为![]() =2mol,11.2 L O2的物质的量为
=2mol,11.2 L O2的物质的量为![]() =0.5mol,物质的物质的量越大,所含分子数越大,则三种物质中所含分子数最多的是氢气,标准状况下,水为固态,则1mol水的体积最小,故答案为:H2;H2O;
=0.5mol,物质的物质的量越大,所含分子数越大,则三种物质中所含分子数最多的是氢气,标准状况下,水为固态,则1mol水的体积最小,故答案为:H2;H2O;
(3)硫酸钾和硫酸铝的混合溶液呈电中性,溶液中存在电荷守恒关系:c(K+)+3c(Al3+)=2c(SO42-),则c(K+)=2×0.7 mol/L—3×0.4 mol/L=0.2 mol/L,故答案为:0.2。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】25℃时,将0.0l mol L -1 NaOH溶液滴入20mL0.01mol·L-1CH3COOH溶液的过程中,溶液中由水电离出的c(H+)与加入NaOH溶液体积的关系如图所示。下列说法正确的是
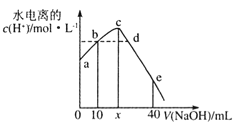
A. x=20,a点的纵坐标为1.0×10-12
B. b点和d点所示溶液的pH相等
C. 滴定过程中,c(CH3COO-)与c(OH-)的比值逐渐增大
D. e点所示溶液中,c(Na+)=2c(CH3COO-)+2c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列氧化还原反应中,水作为还原剂的是( )
A.3Fe+4H2O![]() Fe3O4+4H2B.3NO2+H2O = 2HNO3+ NO
Fe3O4+4H2B.3NO2+H2O = 2HNO3+ NO
C.2Na2O2+2H2O = 4NaOH+O2↑D.2F2+2H2O = 4HF+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图所示),促进了世界制碱技术的发展.下列有关说法正确的是( )
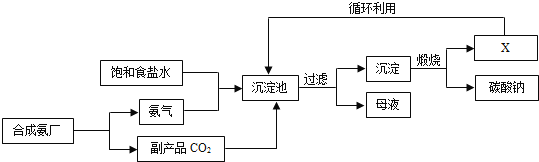
A.沉淀池中的反应物共含有五种元素
B.过滤得到的“母液”中一定只含有两种溶质
C.图中X可能是氨气
D.通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】密闭容器中有如下反应:L(s)+aG(g) ![]() bR(g),温度和压强对该反应的影响如图所示,其中压强p1<p2,由此可判断( )
bR(g),温度和压强对该反应的影响如图所示,其中压强p1<p2,由此可判断( )
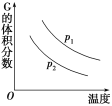
A.正反应为放热反应
B.G的转化率随温度升高而减小
C.化学方程式中的计量数a>b
D.增大压强,容器内气体质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列A、B、C、D是中学常见混合物分离或提纯的基本装置。请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D填入适当的空格中。

(1)除去Ca(OH)2溶液中悬浮的CaCO3_________________;
(2)从碘水提取碘______________;
(3)用自来水制取蒸馏水_________________;
(4)分离植物油和水_____________;
(5)与海水晒盐原理相符的是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应:2A(气)+B(气)![]() 2C(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
2C(气)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法:
①用物质A表示的反应平均速率为0.3 mol·L-1·s-1
②用物质B表示的反应的平均速率为0.6 mol·L-1·s-1
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7 mol·L-1
其中正确的是:
A.①③B.①④C.②③D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。 据此下列说法正确的)

A. 该试剂的物质的量浓度为 9.2 mol·L —1
B. 该硫酸 50 mL 与足量的铜反应可得到标准状况下 SO2 10.3 L
C. 配制 200 mL 4.6 mol·L —1 的稀硫酸需取该硫酸 50 mL
D. 该硫酸与等体积的水混合所得溶液的质量分数小于 49%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲氧基肉桂酸乙基己酯(图中J)是一种理想的防晒剂,能有效吸收紫外线,安全性良好。其合成线路图如下:
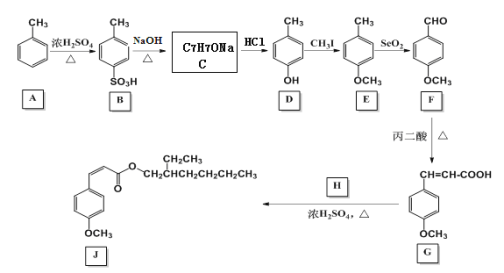
回答下列问题:
(1)由A生成B的反应类型为___。有机物E的分子式为___。丙二酸的结构简式为___。
(2)C的结构简式为___。
(3)H的结构简式为___。
(4)G与氢气反应可得X(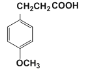 )。X有多种同分异构体,其中同时满足下列条件同分异构体的结构简式为:___。
)。X有多种同分异构体,其中同时满足下列条件同分异构体的结构简式为:___。
①核磁共振氢谱有四种峰;②与FeCl3溶液能发生显色反应,且1mol该物质恰好能与3molNaOH完全反应。
(5)以乙醇和丙二酸为原料合成聚巴豆酸乙酯 ,请补充完成以下合成路线(无机试剂可任选)。
,请补充完成以下合成路线(无机试剂可任选)。
____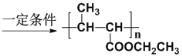
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com