
”¾ĢāÄæ”æ»Æѧ·“Ó¦µÄĖŁĀŹŗĶĻŽ¶Č¶ŌČĖĄąÉś²śÉś»īÓŠÖŲŅŖµÄŅāŅ唣
(1)ŅŃÖŖNa2S2O3£«H2SO4=Na2SO4£«S”ż£«SO2£«H2O”£¼×Ķ¬Ń§Ķعż²ā¶ØøĆ·“Ó¦·¢ÉśŹ±ČÜŅŗ±ä»ė×ĒµÄŹ±¼ä£¬ŃŠ¾æĶā½ēĢõ¼ž¶Ō»Æѧ·“Ó¦ĖŁĀŹµÄÓ°Ļģ£¬Éč¼ĘŹµŃéČēĻĀ(ĖłČ”ČÜŅŗĢå»ż¾łĪŖ2 mL)£ŗ
ŹµŃ鱹ŗÅ | ĪĀ¶Č/”ę | c(Na2S2O3)/mol”¤L£1 | c(H2SO4)/mol”¤L£1 |
¢ń | 25 | 0.1 | 0.1 |
¢ņ | 25 | 0.2 | 0.1 |
¢ó | 50 | 0.2 | 0.1 |
¢ŁÉĻŹöŹµŃéÖŠČÜŅŗ×īĻȱä»ė×ĒµÄŹĒ______£ØĢīŹµŃ鱹ŗÅ£¬ĻĀĶ¬£©”£
¢ŚĪŖĢ½¾æÅØ¶Č¶Ō»Æѧ·“Ó¦ĖŁĀŹµÄÓ°Ļģ£¬Ó¦Ń”Ōń______ŗĶ______”£
(2)ijĪĀ¶ČĻĀ£¬ŌŚ1 LĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦£ŗ2X(g)£«Y(g)![]() 2Z(g)£¬XµÄĪļÖŹµÄĮæĖꏱ¼äµÄ±ä»ÆČēĻĀ±ķ£ŗ
2Z(g)£¬XµÄĪļÖŹµÄĮæĖꏱ¼äµÄ±ä»ÆČēĻĀ±ķ£ŗ
Ź±¼ä/s | 0 | 1 | 2 | 3 | 4 | 5 |
XµÄĪļÖŹµÄĮæ/mol | 0.02 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
¢ŁÓĆXµÄÅØ¶Č±ä»Æ±ķŹ¾0”«2 sµÄĘ½¾ł»Æѧ·“Ó¦ĖŁĀŹĪŖ______mol/(L”¤s)”£
¢ŚŌŚ3 sŅŌŗóXµÄÅØ¶Č²»ŌŁøı䣬·“Ó¦“ļµ½ĮĖ______דĢ¬”£
¢ŪÄÜĖµĆ÷øĆ·“Ó¦ŅŃ“ļµ½»ÆŃ§Ę½ŗāדĢ¬µÄŹĒ______(ĢīŠņŗÅ)”£
A£®vÕż(X)=vÄę(X)
B£®µ„Ī»Ź±¼äÄŚÓŠ2 mol XÉś³ÉĶ¬Ź±ÓŠ1 mol YÉś³É
C£®X”¢Y”¢ZµÄ·Ö×ÓŹżÖ®±ČĪŖ2”Ć1”Ć2
”¾“š°ø”æIII I II 0.006 Ę½ŗāדĢ¬ A
”¾½āĪö”æ
(1)¢Łøł¾ŻÅØ¶Č”¢ĪĀ¶Č¶Ō»Æѧ·“Ó¦ĖŁĀŹµÄÓ°Ļģ“óŠ”·ÖĪöÅŠ¶Ļ£»
¢ŚŅŖĢ½¾æÅØ¶Č¶Ō»Æѧ·“Ó¦ĖŁĀŹµÄÓ°Ļģ£¬Ó¦øĆ²ÉÓĆæŲÖʱäĮæ·½·Ø·ÖĪö£»
(2)¢Łøł¾Ż0”«2 sÄŚXµÄÅØ¶Č±ä»Æ£¬ĄūÓĆĖŁĀŹ¶ØŅåŹ½¼ĘĖć£»
¢Śøł¾ŻæÉÄę·“Ó¦µÄĢŲµćÅŠ¶Ļ£»
¢Ūøł¾ŻĘ½ŗāדĢ¬µÄĢŲÕ÷ÅŠ¶ĻĘ½ŗāדĢ¬”£
(1)¢Łøł¾Ż±ķøńŹż¾ŻæÉÖŖŹµŃéI”¢IIµÄ·“Ó¦ĪĀ¶ČĻąĶ¬£¬ĮņĖįµÄÅضČĻąĶ¬£¬²»Ķ¬µćŹĒNa2S2O3µÄÅØ¶Č²»Ķ¬£»¶ųŹµŃéIIIµÄĪĀ¶ČÓėŹµŃéIIµÄ·“Ó¦ĪĀ¶Č²»Ķ¬£¬ĘäĖüĶā½ēĢõ¼ž¶¼ĻąĶ¬”£ÓÉÓŚĪĀ¶Č¶Ō»Æѧ·“Ó¦ĖŁĀŹµÄÓ°Ļģ“óÓŚÅضČøıä¶Ō»Æѧ·“Ó¦ĖŁĀŹµÄÓ°Ļģ£¬ĖłŅŌ·“Ó¦ĖŁĀŹ×īæģµÄŹĒŹµŃéIII£¬Ņņ“ĖŹµŃéIII×īĻČ¹Ū²ģµ½²śÉśSµ„ÖŹ£¬¶ų³öĻÖ»ė×ĒĻÖĻó£»
¢ŚŅŖĢ½¾æÅØ¶Č¶Ō»Æѧ·“Ó¦ĖŁĀŹµÄÓ°Ļģ£¬Ó¦øĆ²ÉČ”ĻąĶ¬µÄ·“Ó¦ĪĀ¶Č£¬Ö»øıäŅ»ÖÖ·“Ó¦ĪļµÄÅØ¶Č£¬¹Ū²ģÅضČÓė·“Ó¦ĖŁĀŹµÄ¹ŲĻµ”£øł¾Ż±ķøńŹż¾ŻæÉÖŖ£ŗŹµŃéI”¢IIµÄ·“Ó¦ĪĀ¶ČĻąĶ¬£¬ĮņĖįµÄÅضČĻąĶ¬£¬²»Ķ¬µćŹĒNa2S2O3µÄÅØ¶Č²»Ķ¬£¬ŹĒĢ½¾æNa2S2O3µÄÅØ¶Č¶Ō»Æѧ·“Ó¦ĖŁĀŹµÄÓ°Ļģ£¬¹ŹŗĻĄķŃ”ĻīŹĒŹµŃéI”¢II£»
(2)¢Łøł¾Ż±ķøńŹż¾ŻæÉÖŖ£ŗŌŚ0”«2 sÄŚXµÄĪļÖŹµÄĮæ±ä»ÆĮĖ”÷n(X)=0.02 mol-0.008 mol=0.01 2 mol£¬ČŻĘ÷µÄČŻ»żŹĒ1 L£¬ĖłŅŌ”÷c(X)=0.012 mol”Ā1 L=0.012 mol/L£¬¹ŹÓĆXµÄÅØ¶Č±ä»Æ±ķŹ¾µÄ·“Ó¦ĖŁĀŹv(X)=![]() =0.006 mol/(L”¤s)£»
=0.006 mol/(L”¤s)£»
¢ŚæÉÄę·“Ó¦½ųŠŠµÄ×ī“ó³Ģ¶Č¾ĶŹĒ“ļµ½ĮĖøĆĢõ¼žĻĀµÄ»Æѧ·“Ó¦ĻŽ¶Č£¬¼“»ÆŃ§Ę½ŗāדĢ¬£¬“ĖŹ±·“Ó¦ĢåĻµÖŠµÄČĪŗĪĪļÖŹµÄĪļÖŹµÄĮæ²»±ä”£ÓɱķøńŹż¾ŻæÉÖŖŌŚ·“Ó¦½ųŠŠµ½µŚ3 sŹ±£¬XµÄĪļÖŹµÄĮæ²»ŌŁ·¢Éś±ä»Æ£¬ĖµĆ÷“ĖŹ±·“Ó¦“ļµ½ĮĖĘ½ŗāדĢ¬£»
¢ŪA£®ČōvÕż(X)=vÄę(X)£¬ĖµĆ÷XµÄĻūŗÄĖŁĀŹÓė²śÉśĖŁĀŹĻąµČ£¬XµÄÅØ¶Č²»ŌŁ·¢Éś±ä»Æ£¬·“Ó¦“ļµ½ĮĖĘ½ŗāדĢ¬£¬AÕżČ·£»
B£®ÓÉÓŚX”¢Y¶¼ŹĒ·“Ó¦Īļ£¬¶žÕߵĻÆѧ¼ĘĮæŹżµÄ±ČŹĒ2£ŗ1£¬Ņņ“ĖŌŚČĪŗĪĒéæöĻĀ£¬µ„Ī»Ź±¼äÄŚÓŠ2 mol XÉś³ÉĶ¬Ź±ÓŠ1 mol YÉś³É£¬±ķŹ¾µÄ¶¼ŹĒ·“Ó¦ÄęĻņ½ųŠŠ£¬ÓėĘ½ŗāדĢ¬ĪŽ¹Ų£¬B“ķĪó£»
C£®X”¢Y”¢ZµÄ·Ö×ÓŹżÖ®±ČĪŖ2”Ć1”Ć2£¬“ĖŹ±·“Ó¦æÉÄÜ“¦ÓŚĘ½ŗāדĢ¬£¬Ņ²æÉÄÜĪ““¦ÓŚĘ½ŗāדĢ¬£¬ÕāÓė·“Ó¦æŖŹ¼Ź±¼ÓČėµÄ·“Ó¦ĪļµÄ¶ąÉŁ¼°·“Ó¦Ģõ¼žÓŠ¹Ų£¬Ņņ“Ė²»ÄܾŻ“ĖÅŠ¶Ļ·“Ó¦ŹĒ·ńĪŖĘ½ŗāדĢ¬£¬C“ķĪó£»
¹ŹŗĻĄķŃ”ĻīŹĒA”£


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹµŃé·½°øÖŠ£¬ÄÜ“ļµ½ĻąÓ¦ŹµŃéÄæµÄµÄŹĒ
ŹµŃé·½°ø |
|
|
|
|
ÄæµÄ | A£®±Č½ĻŅŅ“¼·Ö×ÓÖŠōĒ»łĒāŌ×ÓŗĶĖ®·Ö×ÓÖŠĒāŌ×ӵĻīĘĆŠŌ | B£®³żČ„ŅŅĻ©ÖŠµÄ¶žŃõ»ÆĮņ | C£®ÖĘŅų°±ČÜŅŗ | D£®Ö¤Ć÷Ģ¼ĖįĖįŠŌĒæÓŚ±½·Ó |
A. A B. B C. C D. D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ²āµĆijĪĀ¶ČĻĀ0.5mol”¤L-1 HNO2£ØŃĒĻõĖį£©ČÜŅŗµÄpHŌ¼ĪŖ2”£
£Ø1£©Š“³öHNO2µÄµēĄė·½³ĢŹ½___”£
£Ø2£©½«ČÜŅŗ¼ÓĖ®Ļ”ŹĶÖĮ10±¶ŗó£¬c(NO2-)___£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©£¬n(H+)___£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©£¬pHĒų¼ä·¶Ī§ŹĒ___”£
A.1”«2 B.2”«3 C.3”«4 D.4”«5
£Ø3£©·Ö±šČ”Ķ¬ÅضČĶ¬Ģå»żµÄŃĪĖįÓėŃĒĻõĖį£¬ŅŌĶ¬ŃłµÄ²Ł×÷Óė×ćĮæNaOHČÜŅŗ·“Ó¦£¬²āµĆ·“Ó¦ČÜŅŗµÄ×īøßĪĀ¶ČŃĪĖįŅŖøßÓŚŃĒĻõĖį£¬ĖµĆ÷æÉÄܵÄŌŅņ___”£
£Ø4£©0.1mol”¤L-1 NaNO2ČÜŅŗpH___7£ØĢī”°£¾”±”¢”°£¼”±»ņ”°£½”±£©£¬ČÜŅŗÖŠŗ¬ÓŠ___ÖÖ·Ö×Ó£¬ČÜŅŗÖŠc(Na+)___c(NO2-)£ØĢī”°£¾”±”¢”°£¼”±»ņ”°£½”±£©£¬ĻĀĮŠ“ėŹ©ÄÜĢįøßČÜŅŗÖŠc(OH-)µÄŹĒ___”£
A.ŹŹµ±ÉżøßĪĀ¶Č B.Ōö¼ÓŃ¹Ēæ C.¼ÓĖ® D.¼ÓČėNH4Cl¹ĢĢå E.¼ÓČėNa2CO3¹ĢĢå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æBodensteins ŃŠ¾æĮĖ·“Ó¦ 2HI(g)![]() I2(g)£« H2(g)£¬Ä³ĪĀ¶ČĻĀ£¬ÉĻŹö·“Ó¦ÖŠ£¬Õż·“Ó¦ĖŁĀŹĪŖ¦ŌÕż=kÕżc2(HI),Äę·“Ó¦ĖŁĀŹĪŖ¦ŌÄę=kÄęc(I2)”¤c(H2),£¬ĘäÖŠkÕż”¢kÄęĪŖĖŁĀŹ³£Źż£¬øł¾ŻŅŌÉĻÄŚČŻµĆ³öµÄ½įĀŪ£¬²»ÕżČ·µÄŹĒ
I2(g)£« H2(g)£¬Ä³ĪĀ¶ČĻĀ£¬ÉĻŹö·“Ó¦ÖŠ£¬Õż·“Ó¦ĖŁĀŹĪŖ¦ŌÕż=kÕżc2(HI),Äę·“Ó¦ĖŁĀŹĪŖ¦ŌÄę=kÄęc(I2)”¤c(H2),£¬ĘäÖŠkÕż”¢kÄęĪŖĖŁĀŹ³£Źż£¬øł¾ŻŅŌÉĻÄŚČŻµĆ³öµÄ½įĀŪ£¬²»ÕżČ·µÄŹĒ
A.·“Ó¦ĪļÅضČŌ½“ó£¬Õż·“Ó¦ĖŁĀŹŌ½“ó
B.Éś³ÉĪļÅضČŌ½“ó£¬Äę·“Ó¦ĖŁĀŹŌ½“ó
C.øĆ·“Ó¦µÄĘ½ŗā³£ŹżK =kÕż/kÄę
D.ĖŁĀŹ³£ŹżµÄ“óŠ”Óė·“Ó¦³Ģ¶ČĪŽ¹ŲĻµ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĶ¼ĪŖŃōĄė×Ó½»»»Ä¤·Øµē½ā±„ŗĶŹ³ŃĪĖ®ŌĄķŹ¾ŅāĶ¼”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
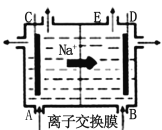
A.“ÓEæŚŅŻ³öµÄĘųĢåŹĒ Cl2
B.ĆæÉś³É 22.4 L Cl2£¬Ķ¬Ź±²śÉś2 mol NaOH
C.“ÓBæŚ¼ÓČėŗ¬ÉŁĮæNaOHµÄĖ®ČÜŅŗŅŌŌöĒæµ¼µēŠŌ
D.ŅĄ“ĪÓĆNa2CO3”¢NaOH”¢BaCl2”¢ŃĪĖįµČŹŌ¼Į³żČ„“ÖŃĪĖ®ÖŠCa2+”¢Mg2+”¢Fe3+”¢SO42£µČĄė×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗĻ³É°±¹¤ŅµŌŚ¹¤Å©ŅµÉś²ś”¢Éś»īÖŠÓŠ×ÅÖŲŅŖ×÷ÓĆ”£·“Ó¦ŌĄķĪŖ£ŗ3H2(g)+N2(g)![]() 2NH3(g) ”÷H < 0”£
2NH3(g) ”÷H < 0”£
£Ø1£©ŌŚT ”ꏱ£¬½«Ņ»¶ØĪļÖŹµÄĮæµÄH2ŗĶN2ÖĆÓŚŅ»ČŻ»ż²»±äµÄĆܱÕČŻĘ÷ÖŠ”£
¢ŁĻĀĮŠø÷ĻīÄÜĖµĆ÷øĆ·“Ó¦ŅŃ“ļµ½Ę½ŗāדĢ¬µÄŹĒ__________(ĢīŠņŗÅ)”£
a.ČŻĘ÷ÄŚµÄŃ¹Ēæ²»ŌŁĖꏱ¼ä±ä»Æ
b.3¦Ō(N2)=¦Ō(H2)
c£®3¦ŌÕż(H2)=2¦ŌÄę(NH3)
d.»ģŗĻĘųĢåµÄĆܶȱ£³Ö²»±ä
¢Ś“ļÉĻŹöĘ½ŗāŗó£¬ĘäĖūĢõ¼ž²»±ä£¬ÉżøßĪĀ¶Č£¬¦ŌÄę___________________(Ģī”°Ōö“ó”±”¢”°²»±ä”±”¢”°¼õŠ””±)£¬¦ŌÕżŗĶ¦ŌÄęµÄ¹ŲĻµĪŖ¦ŌÕż___________¦ŌÄę(Ģī£ŗ”°>”±”¢”°£½”±”¢”°<”±)£¬×īŗó¶žÕßĻąµČ”£
¢ŪøĆĢõ¼žĻĀ“ļµ½Ę½ŗāŹ±£¬ĻņČŻĘ÷ÄŚ³äČė¶čŠŌĘųĢ壬Ōö“óČŻĘ÷ÄŚµÄŃ¹Ē棬NH3µÄĢå»ż·ÖŹż½«(Ģī£ŗ”°±ä“ó”±”¢”°²»±ä”±»ņ”°±äŠ””±)”£________
£Ø2£©ŌŚT ”ꏱ£¬½«Ņ»¶ØĪļÖŹµÄĮæµÄH2ŗĶN2ÖĆÓŚŅ»ČŻ»żæɱäµÄĆܱÕČŻĘ÷ÖŠ”£“ļµ½Ę½ŗāŗó£¬øıäijŅ»Ģõ¼žŹ¹·“Ó¦ĖŁĀŹ·¢ÉśĮĖČēĶ¼ĖłŹ¾µÄ±ä»Æ£¬øıäµÄĢõ¼žæÉÄÜŹĒ______”£
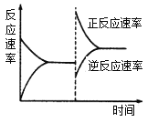
a.ÉżøßĪĀ¶Č£¬Ķ¬Ź±¼ÓŃ¹b.½µµĶĪĀ¶Č£¬Ķ¬Ź±¼õŃ¹
c.±£³ÖĪĀ¶Č”¢Ń¹Ēæ²»±ä£¬Ōö“ó·“Ó¦ĪļÅضČ
d.±£³ÖĪĀ¶Č”¢Ń¹Ēæ²»±ä£¬¼õŠ”Éś³ÉĪļÅضČ
£Ø3£©ŌŚT ”ꏱ£¬½«0.6 mol H2ŗĶ0£®4 mol N2ÖĆÓŚČŻ»żĪŖ2 LµÄĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£ŗ3H2(g)+N2(g)![]() 2NH3 (g) ”÷H <0”£Čō±£³ÖĪĀ¶Č²»±ä£¬Ä³ŠĖȤŠ”×éĶ¬Ń§²āµĆ·“Ó¦¹ż³ĢÖŠČŻĘ÷ÄŚŃ¹Ēæ£ØMPa£©Ėꏱ¼ä±ä»ÆČēĶ¼ĖłŹ¾£ŗ8 minÄŚNH3µÄĘ½¾łÉś³ÉĖŁĀŹĪŖ_______”£
2NH3 (g) ”÷H <0”£Čō±£³ÖĪĀ¶Č²»±ä£¬Ä³ŠĖȤŠ”×éĶ¬Ń§²āµĆ·“Ó¦¹ż³ĢÖŠČŻĘ÷ÄŚŃ¹Ēæ£ØMPa£©Ėꏱ¼ä±ä»ÆČēĶ¼ĖłŹ¾£ŗ8 minÄŚNH3µÄĘ½¾łÉś³ÉĖŁĀŹĪŖ_______”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠµē½āÖŹČÜŅŗÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ
A£®ŗćĪĀĢõ¼žĻĀĻ”ŹĶĒā·śĖįŹ±£¬HFµÄKaŌö“ó£¬Ė®µÄKW²»±ä
B£®ĻņMg(OH)2³ĮµķŠü×ĒŅŗÖŠ¼ÓČėNH4Cl¹ĢĢ壬c£ØMg2£«£©”¢c£ØOH££©ÅØ¶Č¾łŌö“ó
C£®0£®1mol£ÆLNaHCO3ČÜŅŗÖŠ£¬c£ØNa£«£©£¾c£Ø![]() £©£¾c£Ø
£©£¾c£Ø![]() £©£¾c£ØH2CO3£©
£©£¾c£ØH2CO3£©
D£®0£®1mol£ÆLNa2SO3ČÜŅŗÖŠ£¬¼ÓČėÉŁĮæNaOH¹ĢĢ壬c£Ø![]() £©Óėc£ØNa£«£©¾łŌö“ó
£©Óėc£ØNa£«£©¾łŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚŹµŃéŹŅÖŠ£¬æÉŅŌÓŠČēĻĀĮ½ÖÖ·½·ØÖʱø¶žŃõ»ÆĀČ(ClO2)£¬»Ų“šĻĀĮŠĪŹĢā
¢ń.![]()
¢ņ.![]()
(1)NaClO3ÖŠClµÄ»ÆŗĻ¼ŪĪŖ______________”£
(2)¢ńÖŠ»¹Ō²śĪļŹĒ______________”£
(3)¢ņµÄĄė×Ó·½³ĢŹ½ĪŖ__________________________________________£¬Čō·“Ó¦ÖŠÓŠ0.1molµē×Ó×ŖŅĘ£¬Ōņ²śÉśµÄClO2ĘųĢåŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ_____________L”£
(4)¶žŃõ»ÆĀČŹĒŅ»ÖÖŌŚĖ®“¦ĄķµČ·½ĆęÓŠ¹ć·ŗÓ¦ÓƵÄøߊ§°²Č«Ļū¶¾¼Į”£”°ÓŠŠ§ĀČŗ¬Įæ”±æÉÓĆĄ“ŗāĮæŗ¬ĀČĻū¶¾¼ĮµÄĻū¶¾ÄÜĮ¦£¬Ęä¶ØŅåŹĒ£ŗĆææĖŗ¬ĀČĻū¶¾¼ĮµÄŃõ»ÆÄÜĮ¦(µĆŹ§µē×ÓŹż)Ļąµ±ÓŚ¶ąÉŁæĖC12µÄŃõ»ÆÄÜĮ¦(Cl¾ł×Ŗ»ÆĪŖCl-)”£ClO2µÄÓŠŠ§ĀČŗ¬ĮæĪŖ_________________(¼ĘĖć½į¹ū±£ĮōĮ½Ī»Š”Źż)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ»ś·“Ó¦·½³ĢŹ½ŹéŠ“ÕżČ·ĒŅĪŖ¼Ó³É·“Ó¦µÄŹĒ£Ø £©
A.CH4+Cl2![]() CH2Cl2+H2
CH2Cl2+H2
B.CH2=CH2+Br2”śCH3-CHBr2
C.CH2=CH2£«H2O![]() CH3CH2OH
CH3CH2OH
D.![]() +HNO3
+HNO3![]()
![]() +H2O
+H2O
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com