
【题目】某实验过程如图所示,则图③试管中的现象是( ) 
A.铜片溶解,产生无色气体,该气体遇空气变为红棕色
B.铜片溶解,产生无色气体,该气体遇到空气不变色
C.铜片溶解,放出红棕色有刺激性气味的气体
D.无明显现象,因稀硫酸不与铜反应
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述正确的是( ) 
A.反应①为取代反应,有机产物浮在上层
B.反应②为氧化反应,反应现象是火焰明亮并伴有浓烟
C.反应③为取代反应,只生成一种产物
D.反应④中1 mol苯最多与3 mol H2发生加成反应,因为苯分子含有3个碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)电子工业常用FeCl3溶液做腐蚀液制造印刷电路板。用FeCl3做腐蚀液与Cu反应的原理为:2FeCl3+Cu=2FeCl2+CuCl2将一定量铁粉和铜粉的混合物放入等浓度的FeCl3和CuCl2的混合溶液中,可发生多个反应,其中首先发生反应的离子方程式为:。
(2)某校研究性学习小组用已生锈(Fe2O3)的废铁屑制作印刷电路板的腐蚀液(FeCl3溶液),并将刻蚀电路板后的废液再生为FeCl3溶液循环使用。实验流程如下: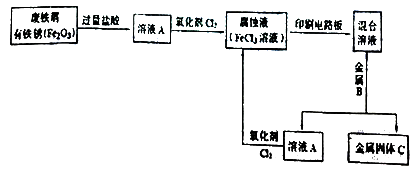
请根据使用流程写出下列反应的离子方程式:
溶液A→腐蚀液:。
混合溶液+金属B→金属固体C:。
(3)检验腐蚀液中Fe3+存在的常用试剂是 , 证明Fe3+存在的现象是。
(4)取适量混合溶液于试管中,加入一定量的铁粉,若反应结束后试管中仍有少量固体,则固体中一定含有 , 溶液中可能含有的金属阳离子是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铁矿(主要成分FeS2)、黄铜矿(主要成分CuFeS2)均是自然界中的常见矿物资源. 
(1)黄铁矿在空气中易被氧化,其反应历程可能为如图1所示的四步: ①a反应中每生成1molFeSO4转移电子的物质的量为mol.
②d反应的离子方程式为 .
(2)用黄铜矿常温细菌冶铜和高温火法冶铜的流程如图2所示: ①细菌冶铜时,当黄铜矿中伴有黄铁矿可明显提高Cu2+的浸出速率,
其原理如图3所示:
Ⅰ.冶炼过程中,FeS2周边溶液的pH(填“增大”、“减小”或“不变”).
Ⅱ.从CuFeS2析出S的反应式是 .
②火法冶铜时,由Cu2S制得铜的化学方程式是 .
(3)煤炭中的硫主要以黄铁矿形式存在,用氢气脱除黄铁矿中硫的相关反应(见表),其相关反应的平衡常数与温度的关系如图4.
相关反应 | 反应热 | 平衡常数 |
FeS2(s)+H2(g)FeS(s)+H2S(g) | △H1 | K1 |
| △H2 | K2 |
FeS(s)+H2(g)Fe(s)+H2S(g) | △H3 | K3 |
①上述反应中,△H10(填“>”或“<”).
②提高硫的脱除率可采取的措施有(举1例).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制取SO2并验证SO2某些性质的装置图。若观察到装置④中有淡黄色沉淀生成,⑤中的溴水褪色(已知因含有Br2而溴水呈红棕色),请回答: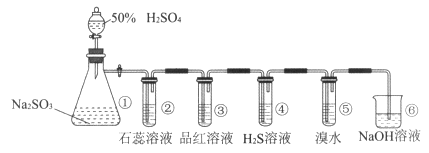
(1)①中发生反应的离子方程式是。
(2)②中的实验现象是。
(3)③的实验现象是 , 证明SO2有性。
(4)④中SO2做剂。
(5)⑤中反应生成两种强酸,该反应的离子方程式是 , 当1 molSO2参与反应时,转移电子的物质的量是。
(6)⑥的作用是。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用如图装置探究SO2的性质. 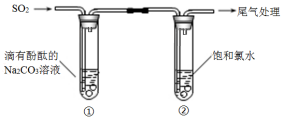
下列有关反应的方程式,不正确的是( )
A.①中溶液显红色的原因:CO32﹣+H2OHCO3﹣+OH﹣
B.①中溶液红色褪去的原因:2SO2+CO32﹣+H2O═CO2+2HSO3﹣
C.②中溶液显黄绿色的原因:Cl2+H2O═HCl+HClO
D.②中溶液黄绿色褪去的原因:SO2+Cl2+2H2O═H2SO4+2HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向200mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2 , 充分反应,测得最后溶液的pH>7.
(1)此时溶液的溶质如果是单一成分,可能是;如果是多种成分,可能是 .
(2)在上述所得溶液中,逐滴缓慢滴加2molL﹣1的盐酸,所得气体(不考虑溶解于水)的体积与所加盐酸的体积关系如图所示:
①加入盐酸200mL之前,无气体产生,写出OA段发生反应的离子方程式 .
②B点时,反应所得溶液中溶质的物质的量浓度是(溶液体积的变化忽略不计).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环扁桃酯是用于治疗心脑血管疾病的重要化合物,它的一种合成路线如图. 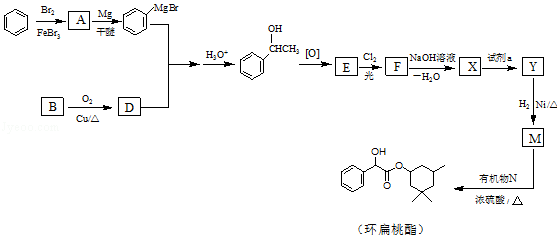
已知: 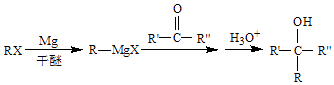 (R、R′、R″代表烃基或氢)
(R、R′、R″代表烃基或氢)
(1)A的结构简式是 .
(2)B→D的化学方程式是 .
(3)红外吸收光谱表明E有C=O键.F的分子式为C8H6Cl2O. ①E的结构简式是 .
②E→F的反应类型是 .
(4)X的结构简式是 .
(5)试剂a是 .
(6)生成环扁桃酯的化学方程式是 .
(7)以CH3CH=CH2、CH3CHO为有机原料,结合题目所给信息,选用必要的无机试剂合成CH2=CHCH=CHCH3 , 写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A是生产生活中用量最大的金属,B为淡黄色粉末。在常温下C为无色液体,E、G、H、I、J为气体,其中H为黄绿色,其它为无色.J能使湿润的红色石蕊试纸变蓝(图中部分产物已略去)。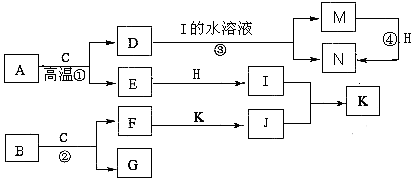
请填写下列空白
(1)写出化学式:M , K。
(2)写出①的化学方程式;写出③的离子方程式。
(3)反应④属于下列何种反应类型______(填字母序号)。
A.化合反应
B.氧化还原反应
C.离子反应
D.置换反应
(4)若要确定③反应后所得溶液中含有M物质,所选试剂为______(填序号)。
A.KSCN溶液和氯水
B.铁粉和KSCN
C.浓氨水
D.酸性高锰酸钾溶液
(5)常温下,H与过量的J反应产生浓厚的白烟,另一生成物是空气的主要成分之一,请写出该反应的化学方程式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com