
【题目】科学家研制的一种使沙漠变绿洲的新技术,即在沙漠中喷洒一定量的聚丙烯酸酯与水的混合物,使其与沙粒结合,形成既能阻止地下的盐分上升,又能拦截、蓄积雨水的作用。下列对聚丙烯酸酯的叙述中正确的是( )
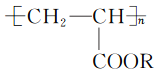
①聚丙烯酸酯的单体的结构简式为CH2=CHCOOR
②聚丙烯酸酯没有固定的熔沸点
③聚丙烯酸酯能发生加成反应
④合成聚丙烯酸酯的反应属于缩聚反应
A. ③④ B. ①② C. ①②③ D. ①②③④
科目:高中化学 来源: 题型:
【题目】周期表是一座开放的“元素大厦”,元素大厦尚未客满。请你在元素大厦中为119号元素安排好它的房间( )
A. 第八周期第IA族 B. 第七周期第ⅦA族
C. 第七周期第0族 D. 第六周期ⅡA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于Na2CO3和NaHCO3性质的说法正确的是( )
A.等浓度时水溶液碱性:NaHCO3>Na2CO3
B.热稳定性:NaHCO3>Na2CO3
C.与盐酸溶液反应的速率(快慢):NaHCO3<Na2CO3
D.等质量的Na2CO3、NaHCO3分别与足量的盐酸反应,NaHCO3产生的CO2多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤燃烧产生的粉煤灰(主要含有SiO2、Fe2O3、Al2O3等)是火电厂产生的废渣,若不加处理会污染环境。为综合利用,研究人员对其进行如下处理:
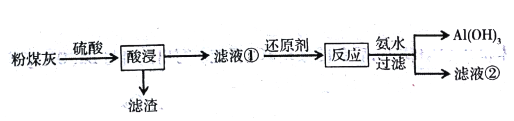
(1)滤渣主要成分是________________;滤液①中的阳离子为_____________________。
(2)滤液①中还加入还原剂原因是________________;若加入的还原剂为铁粉,反应的离子方程式为_____________________________________。
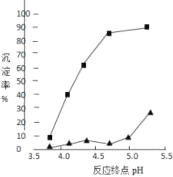
(3)加入氨水是为了调节pH使铝离子沉淀,其离子方程式为_________________;反应终点的pH对铝和铁分离效果的影响如右图。根据实验结果,为达到好的分离效果,反应过程中控制pH的范围是__________,选择该范围的理由是_________。
(4)NH4HSO4和H2SO4按物质的量比1:1混合溶于水配制成浸取液,220℃时可将高铝粉煤灰中Al2O3转化为硫酸铝铵[NH4Al(SO4) 2],然后分离、煅烧获得纯Al2O3。
查阅资料知硫酸铝铵:①溶解度:0℃时,S=5.2g;100℃时,S=421.9g 。②280℃时分解。
①依据资料可知,将硫酸铝铵与其他溶质分离的方法是_____________。
②煅烧NH4Al(SO4)2时发生4NH4Al(SO4)2![]() 2Al2O3+5SO3↑+3SO2↑+2NH3↑+N2↑+5H2O↑,得到混合气体(NH3、N2、SO2、SO3、H2O)。若16mol混合气体按如下装置被完全吸收制得浸取液。则右下图中,试剂X是___________(填化学式);试剂Y是_________(填名称),其中溶质的物质的量为_____________。
2Al2O3+5SO3↑+3SO2↑+2NH3↑+N2↑+5H2O↑,得到混合气体(NH3、N2、SO2、SO3、H2O)。若16mol混合气体按如下装置被完全吸收制得浸取液。则右下图中,试剂X是___________(填化学式);试剂Y是_________(填名称),其中溶质的物质的量为_____________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mg·L-1。我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于5 mg·L-1。水中溶解氧的测定步骤如下:
(1)向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;
(2)加入适量稀H2SO4,搅拌,等MnO(OH)2与I-完全反应生成Mn2+和I2后;
(3)用Na2S2O3标准溶液滴定至终点。
测定过程中物质的转化关系如下:

已知:MnO(OH)2+2I-+4H+ =Mn2++I2+3H2O 2S2O32- +I2= S4O62-+2I-
①加入稀硫酸后搅拌的作用是__________;Na2S2O3标准溶液应装在______________滴定管中(填酸式或碱式)。
②滴定过程中以_____________为指示剂;达到滴定终点的标志为____________________。
③写出O2将Mn2+氧化成MnO(OH)2的离子方程式____________________;
④若加入的稀H2SO4溶液反应后,若溶液pH过低,滴定时会产生明显的误差。写出产生误差的一个原因(用离子方程式表示)__________________。
⑤下列操作使测得水样中溶氧量(DO)比实际值偏高的是__________________。
A.第(1)步操作静置时没有密封 B.装Na2S2O3标准溶液的滴定管没有润洗
C.滴定前锥形瓶洗净后没有干燥 D.滴定前读数正确,滴定后俯视读数
⑥取加过一定量CaO2·8H2O的池塘水样l00.00mL,按上述方法测定水中溶解氧量,消耗0.01000
mol·L-1 Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧为____________mg·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20mL 0.5mol/L的盐酸与一块大理石反应,下列措施不能提高反应速率的是 ( )
A. 加入10mL 1mol/L的盐酸 B. 加入30mL 10mol/L的盐酸
C. 加入10mL H2O D. 所用的大理石研磨成粉末
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等质量的两块钠,第一块钠在足量氧气中加热,第二块钠放置在空气中,待反应完全后,下列说法正确的是( )
A. 第一块钠失去的电子多
B. 两块钠失去的电子一样多
C. 第二块钠的反应产物质的量较大
D. 两块钠的反应产物质量一样大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com