
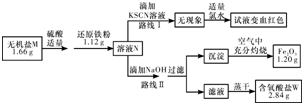
·ÖĪö 1.2gŃõ»ÆĢśµÄĪļÖŹµÄĮæĪŖ£ŗ$\frac{1.2g}{160g/mol}$=0.0075mol£¬ŌņČÜŅŗNÖŠŗ¬ÓŠĢśŌŖĖŲµÄĪļÖŹµÄĮæĪŖ£ŗ0.0075mol”Į2”Į2=0.03mol£¬ÖŹĮæĪŖ£ŗ56g/mol”Į0.03mol=1.68g£¾1.12g£¬ĖłŅŌĪŽ»śŃĪMÖŠŅ»¶Øŗ¬ÓŠFeŌŖĖŲ£¬¹ŹŌĄ“ĪŽ»śŃĪMÖŠĢśŌŖĖŲµÄĪļÖŹµÄĮæĪŖ0.03mol-0.02mol=0.01mol£»¾ŻĢāŅāµĆEĪŖNa2SO4£¬2.84g Na2SO4ĪļÖŹµÄĮæĪŖ0.02mol£¬¹ŹĪŽ»śŃĪWÖŠŗ¬ÄĘŌŖĖŲ£¬ŅĄ¾ŻWĪŖŗ¬ŃõĖįøł£¬ĒŅ·Ö×ÓÖŠµÄŌ×ÓøöŹż±ČĪŖ1£ŗ2£ŗ4£¬æɵĆMµÄ»ÆѧŹ½ĪŖK2FeO4£¬
¢ŁĀ·ĻߢńĪŖ¼ģŃéŃĒĢśĄė×ӵķ½·Ø£»
¢ŚK2FeO4ÓėĻ”ĮņĖį”¢Ģś·Ū·“Ӧɜ³ÉĮņĖįŃĒĢś”¢ĮņĖį¼ŲŗĶĖ®£¬øł¾ŻÖŹĮæŹŲŗćæÉÖŖWĪŖĮņĖį¼Ų£»
¢Ūøł¾ŻK2FeO4ÓėĻ”ĮņĖį”¢Ģś·Ū·“Ӧɜ³ÉĮņĖįŃĒĢś”¢ĮņĖį¼ŲŗĶĖ®Š“³ö·“Ó¦µÄ»Æѧ·½³ĢŹ½£®
½ā“š ½ā£ŗ¢Łøł¾ŻĀ·ĻߢńæÉÖŖ£¬NČÜŅŗÖŠŅ»¶Øŗ¬ÓŠŃĒĢśĄė×Ó£¬¹Ź“š°øĪŖ£ŗFe2+£»
¢Ś1.2gŃõ»ÆĢśµÄĪļÖŹµÄĮæĪŖ£ŗ$\frac{1.2g}{160g/mol}$=0.0075mol£¬ŌņČÜŅŗÖŠŗ¬ÓŠĢśŌŖĖŲµÄĪļÖŹµÄĮæĪŖ£ŗ0.0075mol”Į2”Į2=0.03mol£¬ÖŹĮæĪŖ£ŗ56g/mol”Į0.03mol=1.68g£¾1.12g£¬ĖłŅŌĪŽ»śŃĪMÖŠŅ»¶Øŗ¬ÓŠFeŌŖĖŲ£¬ĪŽ»śŃĪM·Ö×ÓÖŠµÄŌ×ÓøöŹż±ČĪŖ1£ŗ2£ŗ4£¬ŌņMµÄ»ÆѧŹ½ĪŖ£ŗNa2FeO4£¬øł¾ŻĮ÷³ĢæÉÖŖ£¬Na2FeO4ÓėĻ”ĮņĖį”¢»¹ŌĢś·Ū·“Ӧɜ³ÉĮņĖįŃĒĢśŗĶĮņĖį¼Ų£¬øł¾ŻÖŹĮæŹŲŗćæÉÖŖWĪŖĮņĖį¼Ų£¬
¹Ź“š°øĪŖ£ŗNa2SO4 £»
¢Ū1.66gNa2FeO4µÄĪļÖŹµÄĮæĪŖ0.01mol£¬1.12g»¹ŌĢś·ŪµÄĪļÖŹµÄĮæĪŖ0.02mol£¬ĖłŅŌNa2FeO4Óė»¹ŌĢś·Ū°“ĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ2·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2Fe+FeO42-+8H+ØT3Fe2++4H2O£¬
¹Ź“š°øĪŖ£ŗ2Fe+FeO42-+8H+ØT3Fe2++4H2O£®
µćĘĄ ±¾Ģāæ¼²éĮĖĢ½¾æĪļÖŹ×é³ÉµÄ·½·Ø£¬ĢāÄæÄŃ¶Č½Ļ“ó£¬ŹŌĢāÉę¼°ĪļÖŹ×é³ÉµÄ²ā¶Ø”¢ÅØĮņĖįµÄŠŌÖŹ”¢Ąė×Ó·½³ĢŹ½”¢»Æѧ·½³ĢŹ½µÄŹéŠ“”¢Ąė×ӵļģŃé·½·ØµČÖŖŹ¶£¬ŹŌĢāÖŖŹ¶µć½Ļ¶ą£¬×ŪŗĻŠŌ½ĻĒ棬³ä·Öæ¼²éĮĖѧɜĮé»īÓ¦ÓĆ»ł“”ÖŖŹ¶µÄÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH4+”¢Ba2+”¢NO3-”¢CO32- | B£® | Fe2+”¢OH-”¢SO42-”¢MnO4- | ||
| C£® | Na+”¢Mg2+”¢NO3-”¢SO42- | D£® | Na+”¢Fe3+”¢Cl-”¢AlO2- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓƶžŃõ»ÆĮņĘÆ°×Ö½½¬”¢Ć«”¢Ė攢²ŻĆ±±čµČ£¬ŹĒŅņĪŖ¶žŃõ»ÆĮņµÄ»¹ŌŠŌÄÜŹ¹ÓŠÉ«ĪļÖŹ±»Ńõ»Æ¶ųĶŹÉ« | |
| B£® | ¹żŃõ»ÆÄĘÓĆÓŚŗōĪüĆę¾ß×÷ĪŖŃõĘųµÄĄ“Ō“£¬ŹĒŅņĪŖ¹żŃõ»ÆÄĘ¾ßÓŠĒæŃõ»ÆŠŌÄÜŃõ»Æ¶žŃõ»ÆĢ¼ ŗųĖ®Éś³ÉŃõĘų | |
| C£® | ĻņŃĪ¼īµŲ£Øŗ¬½Ļ¶ąµÄNaCl”¢Na2C03£©ÖŠŹ©¼ÓŹŹĮæŹÆøą£¬æɽµµĶĶĮČĄµÄ¼īŠŌ£¬ŹĒŅņĪŖŹÆøąÄÜÓė Na2C03·“Ӧɜ³ÉCaC03³Įµķ | |
| D£® | ŌŚ±»±£»¤µÄ¹ųĀÆÄŚ±Ś£¬×°ÉĻĆ¾ŗĻ½š»ņŠææ飬ŅŌ¼õÉŁ¹ųĀƵÄøÆŹ“£¬ŹĒŅņĪŖĆ¾”¢Šæ±ČĢś»īĘĆ£¬ÕāŃłĮ¬½ÓŹ¹¹ųĀÆ×öĪŖŌµē³ŲµÄøŗ¼«±»±£»¤ĻĀĄ“ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

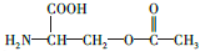 £®
£® b£®ŌŚĻ”ĮņĖįÖŠĖ®½āÓŠŅŅĖįÉś³É
b£®ŌŚĻ”ĮņĖįÖŠĖ®½āÓŠŅŅĖįÉś³É £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ³£ĪĀ³£Ń¹ĻĀ£¬1 L 1 mol•L-1µÄBaCl2ČÜŅŗÖŠÓŠNAøöCl- | |
| B£® | 1 mol Fe±»ĶźČ«Ńõ»ÆÉś³ÉFe3O4£¬Ź§Č„8 NAøöµē×Ó | |
| C£® | ³£ĪĀ³£Ń¹ĻĀ£¬14 gµÄCOŗĶN2»ģŗĻĘųĢåŗ¬ÓŠµÄŌ×ÓŹżĪŖNA | |
| D£® | ³£ĪĀ³£Ń¹ĻĀ£¬22.4 LŃõĘųÓė×ćĮæĆ¾·Ū³ä·Ö·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ2NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 112 mL | B£® | 224 mL | C£® | 448 mL | D£® | 560 mL |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com