
向用盐酸酸化的MgCl2、FeCl3混合溶液中逐滴滴入NaOH溶液,生成的沉淀质量与滴入NaOH溶液体积关系如右图,则原混合溶液中MgCl2与FeCl3的物质的量之比为( )
A. B.
B.

C.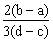 D.
D.
 金钥匙试卷系列答案
金钥匙试卷系列答案科目:高中化学 来源: 题型:
A、B、C、X是中学化学常见物质,均由短
周期元素组成,转化关系如图。
请针对以下三种不同情况回答:
(1)若A、B、C中均含同一种常见金属元素,该元素
 在C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀。
在C中以阴离子形式存在,将A、C的水溶液混合可得B的白色胶状沉淀。
①A中含有的金属元素在元素周期表中的位置为__________,向水中加入X物质,X对水的电离平衡的影响是 (填“促进”、“抑制”或 “无影响”) 。
②A与C的水溶液混合后生成B反应的离子方程式为 。
(2)若A为固态非金属单质,A与X同周期,同时A在X中燃烧,产生白色烟雾,常温常压下C为白色固体,B分子中各原子最外层均为8电子结构。
①若A为该元素的白色固体单质,则1mol A单质中含共价键数目为 NA ,B的电子式为___________。
②X与水反应的离子方程式为 。
(3)若A、B、C的焰色反应呈黄色,水溶液均为碱性,常温下,X为气态酸性氧化物。
①A中所含有的化学键类型是_____________________。
②C溶液中离子浓度由小到大的顺序是__ _________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E是元素周期表中半径最小的元素。请回答下列问题:
(1)X、Y的元素符号依次为 、 ;
(2)XZ2与YZ2分子的立体结构分别是 和 ,
相同条件下两者在水中的溶解度较大的是 (写分子式).
(3)Q的元素核外价层电子排布式为 .
(4)XE2中X原子的杂化方式为 ;Y与E形成的化合物种类很多,其中有一种化合物分子中有6个原子,且6个原子共平面,该化合物名称为 。
(5)在Y2E6Z中存在 种结构,写出其中一种具有对称结构的结构式
查看答案和解析>>
科目:高中化学 来源: 题型:
下列判断正确的是 ( )
A.离子键被破坏的变化一定是化学变化。
B.含有金属阳离子的晶体中一定有阴离子
C.分子晶体中分子间作用力越大,分子越稳定
D.NaCl熔化时离子键被破坏,冰熔化时分子中共价键没有断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。已知:C3H8(g)+5O2(g)—→3CO2(g)+4H2O(l)+2220.0kJ
C3H6(g)+4.5O2(g)—→3CO2(g)+3H2O(l)+2049kJ
下列说法正确的是( )。
A. 1molC3H8(g)与5molO2(g)反应生成3molCO2(g)和4molH2O(g)放出热量大于2220.0kJ
B. 1molC3H6与4.5molO2反应生成3molCO2和3molH2O放出热量等于2049.0kJ
C. 丙烷分子储存的能量大于丙烯分子
D. 丙烷转化为丙烯的过程是一个吸热过程
查看答案和解析>>
科目:高中化学 来源: 题型:
为测定碳酸氢钠纯度(含有少量氯化钠),学生设计了如下几个实验方案(每个方案均称取m1 g样品),请回答每个方案中的问题。
[方案I]选用重量法进行测定:可用下图中的装置进行实验。

(1)A装置中NaOH溶液的作用是__________ _______,若直接向试样溶液中鼓人空气会导致实验测定结果________(填“偏高”、“偏低”或“无影响”)
(2)该方案需直接测定的物理量是 。
[方案II]选用滴定法进行测定:
 (3)称取m1 g样品,配成100mL溶液,取出20mL,用cmol/L的标准HCl溶液滴定,消耗体积为v mL,则该试样中碳酸氢钠质量分数的计算式为:
(3)称取m1 g样品,配成100mL溶液,取出20mL,用cmol/L的标准HCl溶液滴定,消耗体积为v mL,则该试样中碳酸氢钠质量分数的计算式为:
[方案III]选用气体体积法进行测定:可用右图中的装置进行实验。
(4)为了减小实验误差,量气管中加入的液体X为
(5)通过实验,测得该试样中碳酸氢钠质量分数偏低,产生这种现象的原因可能是_________
a.测定气体体积时未冷却至室温
b.测定气体体积时水准管的水面高于量气管的水面
c.Y型管中留有反应生成的气体
d.气体进入量气管前未用浓硫酸干燥
[方案IV]其操作流程如下:
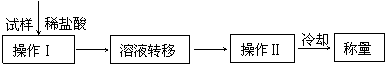
(6)操作Ⅱ的名称是________________________
(7)实验中需要的仪器有电子天平、蒸发皿、玻璃棒等,还需要的玻璃仪器是 ,
(8)在转移溶液时,如溶液转移不完全,则碳酸氢钠质量分数的测定结果_________(填“偏高”、“偏低”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物的结构简式如图所示。1 mol该有机物与足量的NaOH溶液共热,充分反应后最多可消耗NaOH的物质的量为( )

A.2 mol B.6 mol C.8 mol D.4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
铍元素性质与铝元素性质相似,下列方法能证明氯化铍由共价键构成的是( )
A.溶于水加硝酸银溶液,观察是否有白色沉淀生成
B.溶于水做导电实验,观察是否导电
C.熔融状态,做导电实验,观察是否导电 D.测定氯化铍熔点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com