
【题目】工业上曾经通过反应“3Fe + 4NaOH![]() Fe3O4 + 2H2↑+ 4Na↑”生产金属钠。下列说法正确的是
Fe3O4 + 2H2↑+ 4Na↑”生产金属钠。下列说法正确的是
A. 还原产物是钠Na和Fe3O4
B. 用磁铁可以将Fe与Fe3O4分离
C. 将生成的气体在空气中冷却可获得钠
D. 每生成1 mol H2,该反应转移的电子数约为4×6.02×1023
【答案】D
【解析】
A.在该反应中,Na元素的化合价由反应前NaOH中的+1价变为反应后Na单质的0价,化合价降低,获得电子,被还原,所以还原产物是Na;Fe元素的化合价由反应前Fe单质的0价变为反应后Fe3O4中的+2、+3价,化合价升高,失去电子,被氧化,所以Fe3O4是氧化产物,A错误;
B. Fe与Fe3O4都可以被磁铁吸引,所以不能用磁铁可以将Fe与Fe3O4分离,B错误;
C.钠极易被空气中的氧气氧化,所以将生成的气体在空气中冷却得不到钠,C错误;
D.根据方程式可知:每生成2 mol H2,转移8mol的电子,则生成1molH2,转移电子的物质的量为4mol,电子数目约为4×6.02×1023, D正确;
故合理选项是D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】有机物的结构可用键线式简化表示,如CH3-CH=CH-CH3可表示为![]() ,有一种有机物X的键线式如图所示。
,有一种有机物X的键线式如图所示。

(1)X的分子式为_______________________。
(2)有机物Y是X的同分异构体,且属于芳香族化合物。则Y的结构简式是_____________。
(3)Y在一定条件下可发生反应生成高分子化合物,该反应的化学方程式是_________________。
(4)Y可以与溴水反应,该反应的化学方程式是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究一溴环己烷(![]() )与NaOH的醇溶液共热发生的是水解反应还是消去反应,甲、乙、丙三位同学分别设计如下三个实验方案:
)与NaOH的醇溶液共热发生的是水解反应还是消去反应,甲、乙、丙三位同学分别设计如下三个实验方案:
甲:向反应混合液中滴入稀硝酸中和NaOH,然后再滴入AgNO3溶液,若有浅黄色沉淀生成则可证明发生了消去反应。
乙:向反应混合液中滴入溴水,若溶液颜色很快褪去,则可证明发生了消去反应。
丙:向反应混合液中滴入酸性KMnO4溶液,若溶液颜色变浅,则可证明发生了消去反应。
其中正确的是( )
A. 甲 B. 乙 C. 丙 D. 上述实验方案都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.1 mol·L-1NaHCO3与0.1 mol·L-1NaOH等体积混合所得的溶液中,粒子的物质的量浓度关系不正确的是( )
A.c(Na+)>c(CO32-)>c(HCO3-)>c(H2CO3)
B.c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)]
C.c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3)
D.c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿(CuFeS2)是炼铜的最主要矿物。火法冶炼黄铜矿的过程中,其中一步反应是;2Cu2O+ Cu2S![]() 6Cu+SO2。回答下列问题。
6Cu+SO2。回答下列问题。
(1)Cu+的价电子轨道表示式为__________________;Cu2O与Cu2S比较,熔点较高的是_______,原因为_____________________________________。
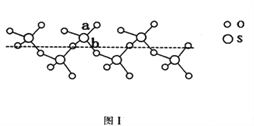
(2)SO2与SO3的键角相比,键角更大的是____________。将纯液态SO3冷却到289.8K时凝固得到一种螺旋状单链结构的固体,其结构如下图1所示。此固态SO3中S原子的杂化轨道类型是_______;该结构中S—O键长有两类,一类键长约140pm,另一类键长约为160pm,较短的键为_________(填图中字母)。
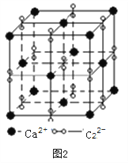
(3)离子化合物CaC2的一种晶体结构如下图2所示。写出该物质的电子式_____。从钙离子看,属于____________堆积;一个晶胞含有的π键平均有______个。

(4)奥氏体是碳溶解在γ—Fe中形成的一种间隙固溶体,无磁性,其晶胞如上图3所示,则该物质的化学式为________,若晶体密度为dg/cm3,则晶胞中最近的两个碳原子的距离为____________________ pm。(阿伏加德罗常数的值用NA表示,写出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁的氧化物极为复杂。为测定一种铁的氧化物样本X的化学式,实验过程如下:

根据实验结果,该氧化物X的化学式为
A. Fe2O3 B. Fe3O4 C. Fe4O5 D. Fe5O7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一定量含有Na2O杂质的Na2O2试样,用如图的实验装置测定Na2O2试样的纯度。
回答下列问题:

(1)装置A中盛放稀盐酸的仪器名称为__________________。
(2)装置B的作用是______________________________________。
(3)装置C的作用是____________________________________________。
(4)装置D中发生反应的化学方程式是_____________、_______________。
(5)装置E中碱石灰的作用是______________________________________。
(6)若开始时称得样品的质量为4.52 g,反应结束后称得固体的质量为6.36g,则Na2O2试样的纯度为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如表提供的数据可知,在溶液中能大量共存的微粒组是

A. H2CO3 、HCO3-、CH3COO-、CN-
B. CO32-、 HCO3-、CH3COOH、CN-
C. HCO3-、CH3COO-、CN-、HCN
D. HCN 、HCO3-、CN-、CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com