
| A. | 第二周期元素从左到右,最高正价从+1递增到+7 | |
| B. | ⅠA和ⅦA族元素间可形成离子化合物和共价化合物 | |
| C. | 同主族元素的简单阴离子还原性越强,元素非金属性越强 | |
| D. | 同周期金属元素的化合价越高,其金属性越强 |
分析 A.主族元素族序数与其最高正化合价相等,但O、F元素没有正化合价;
B.第IA族和第VIIA族元素可能形成离子键化合物或共价化合物;
C.同一主族元素的简单阴离子还原性越强,该非金属元素非金属性越弱;
D.同一周期金属元素的化合价越高,其金属性越弱.
解答 解:A.主族元素族序数与其最高正化合价相等,因为O、F元素电负性较大,导致O、F元素没有正化合价,故A错误;
B.第IA族和第VIIA族元素可能形成离子键化合物或共价化合物,如HCl、NaCl等,故B正确;
C.同一主族元素的简单阴离子还原性越强,该非金属元素得电子能力越弱,所以其非金属性越弱,故C错误;
D.主族元素族序数与其最高正化合价相等,同一周期金属元素的化合价越高,其原子序数越大,则金属性越弱,故D错误;
故选B.
点评 本题考查同一周期同一主族元素性质递变规律,侧重考查元素周期律知识,明确元素周期律内涵是解本题关键,注意规律中的异常现象,异常现象是A.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题

| 物质 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 | Mn(OH)2/Mn(OH)3 |
| 开始沉淀pH | 2.7 | 7.6 | 5.7 | 8.3 |
| 完全沉淀pH (c≤1.0×10-5mol/L) | 3.7 | 9.6 | 8.0 | 8.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{6}^{12}$C、${\;}_{6}^{13}$C、${\;}_{6}^{14}$C是碳元素的三种核素 | |
| B. | SO2分子中含有离子键 | |
| C. | MgCl2固体中含有共价键 | |
| D. | ${\;}_{8}^{16}$O、${\;}_{8}^{17}$O、${\;}_{8}^{18}$O含有相同的中子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 周期 族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
| 4 | ⑪ | ⑫ |
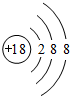 ;最活泼的非金属元素的离子结构示意图
;最活泼的非金属元素的离子结构示意图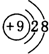 ;最活泼金属元素过氧化物的电子式
;最活泼金属元素过氧化物的电子式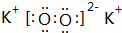 ,指出其中的化学键类型离子键、共价键;①的最高价氧化物的结构式O=C=O.
,指出其中的化学键类型离子键、共价键;①的最高价氧化物的结构式O=C=O.| 实验步骤 | 实验现象与结论 |
| 向H2S溶液中通入O2 | 溶液出现浑浊,说明O2的氧化性比S强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K 1s22s22p63s23p64s1 | B. | Mg2+ 1s22s22p6 | ||
| C. | F- 1s22s22p5 | D. | Br 1s22s22p63s23p63d104s24p5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CHO | B. | 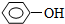 | C. | CH2=CH2 | D. | HOOCCH=CH2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com