
| A. | 在相同温度下,甲酸溶液比盐酸溶液的导电性弱 | |
| B. | 甲酸能与NaHCO3作用放出CO2气体 | |
| C. | 等体积、等物质的量浓度甲酸溶液与NaOH溶液混合时恰好完全中和 | |
| D. | 室温下,1mol/L的甲酸溶液的pH=2 |
分析 A.没有告诉甲酸与盐酸的浓度相等,则无法根据导电性判断甲酸是否为弱电解质;
B.该反应只能说明甲酸酸性大于碳酸,但不能说明甲酸部分电离;
C.甲酸与氢氧化钠为酸碱之间的中和反应,不能判断强弱电解质;
D.1mol/L的甲酸溶液的pH约为2,说明甲酸在溶液中部分电离出氢离子.
解答 解:A.甲酸溶液的导电性比盐酸的弱,只能说明甲酸中离子浓度大于盐酸,不能说明甲酸部分电离,所以不能证明甲酸是弱电解质,可以根据相同浓度的甲酸、盐酸导电性强弱判断甲酸是否是弱电解质,故A错误;
B.甲酸能和NaHCO3作用放出CO2气体,说明甲酸酸性大于碳酸,但不能说明甲酸部分电离,所以不能说明甲酸是弱电解质,故B错误;
C.等体积等浓度的甲酸和NaOH溶液恰好完全反应,说明甲酸是一元酸,不能说明甲酸部分电离,则不能证明甲酸是弱电解质,故C错误;
D.1mol•L-1的甲酸溶液的pH约为2,溶液中氢离子浓度小于甲酸浓度,所以甲酸部分电离,为弱电解质,故D正确;
故选D.
点评 本题考查了弱电解质的电离平衡及其应用,题目难度中等,注意明确电解质强弱是根据电离程度划分的,不能直接根据溶液导电性强弱判断,易错选项是A.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
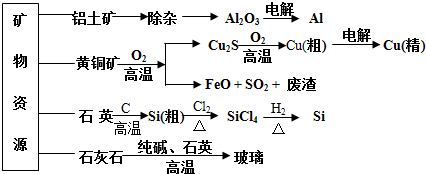
| A. | 制取玻璃的同时产生CO2气体,制取粗硅时生成的气体产物为CO | |
| B. | 黄铜矿冶炼铜时产生的SO2可用于生产硫酸,FeO可用作冶炼铁的原料 | |
| C. | 粗硅制高纯硅时,提纯四氯化硅可用多次蒸馏的方法 | |
| D. | 生产高纯硅、铝、铜及玻璃的过程中都涉及氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2晶体中每个硅原子与两个氧原子以共价键相结合 | |
| B. | 金属晶体的熔点都比分子晶体的熔点高 | |
| C. | 金刚石的晶胞中含有4个碳原子 | |
| D. | NaCl晶体中与每个Na+距离相等且最近的Na+共有12个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;
; 、
、 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com