
| A | B | C | |
| 浓度1 | 0.05mol•L-1 | amol•L-1 | 0.05mol•L-1 |
| 浓度2 | 0.078mol•L-1 | 0.078mol•L-1 | 0.122mol•L-1 |
| 浓度3 | 0.06mol•L-1 | 0.06mol•L-1 | 0.04mol•L-1 |
| 浓度4 | 0.07mol•L-1 | 0.07mol•L-1 | 0.098mol•L-1 |
| A. | 由[浓度3]与[浓度1]的比较,可判断出正反应是放热反应 | |
| B. | 由[浓度2]与[浓度1]的比较,可判断平衡移动的原因是升高温度 | |
| C. | [浓度1]中a=0.05mol•L-1 | |
| D. | 该组某学生在实验①过程中,测得各物质在某一时刻的浓度为[浓度4].与[浓度1]比较,可发现该同学在测定[浓度4]这组数据时出现了很大的误差 |
分析 A、根据[浓度2]与[浓度1]中的浓度变化判断正反应是吸热还是放热反应;
B、根据[浓度3]与[浓度1]中反应物、生成物浓度变化分析是增大压强还是减小压强;
C、根据反应的方程式A(g)+B(g)?C(g)+D(s)来判断,在恒温条件下往一个容积为10L的密闭容器中充入1molA和1molB,反应达平衡时,第Ⅰ组消耗的B的物质的量与A的物质的量相等;
D、根据等效平衡和极性转化法进行判断.
解答 解:A、升高温度后,反应物A、B的浓度增大,C的浓度减小,说明化学平衡向着逆向移动,可判断出正反应是放热反应,故A正确;
B、由于D是固体,该反应在正反应是体积缩小的反应,由[浓度3]与[浓度1]的比较,[浓度3]反应物浓度增加、生成物浓度减小,平衡向着逆向移动,说明是减小了压强,故B错误;
C、反应A(g)+B(g)?C(g)+D(s)中,A和B加入的物质的量相等,化学计量数相等,所以反应达平衡时,第Ⅰ组消耗的B的物质的量与A的物质的量相等,故a=0.05,故C正确;
D、将C的浓度完全转化成A、B的浓度,A、B的浓度都为0.168mol/L,物质的量为1.68mol,最初加入的A、B的物质的量均为1mol,显然在测定过程中出现了很大误差,故D正确;
故选B.
点评 本题考查了影响化学平衡的因素,题目难度中等,充分考查了学生的分析、理解能力和灵活应用所学知识的能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
| 相对分 子质量 | 密度 (g•cm-3) | 沸点 ℃ | 溶解性 | |
| 环己 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③⑥ | B. | ③⑥ | C. | ①②④ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “APEC蓝”是2014年新的网络词汇,形容2014年APEC会议期间北京蓝蓝的天空.说明京津冀实施道路限行和污染企业停工等措施,对减轻雾霾、保证空气质量是有效的 | |
| B. | “地沟油”经过加工处理后,可以用来制肥皂和生物柴油 | |
| C. | 生石灰、铁粉、硅胶是食品包装中常用的干燥剂 | |
| D. | 有机垃圾发酵生产沼气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在一定条件下,将1.00molN2(g)与3.00molH2(g)混合于一个10.0L密闭容器中,在不同温度下达到平衡时NH3(g)的平衡浓度如图所示.其中温度为T1时平衡混合气体中氨气的体积分数为25.0%.
在一定条件下,将1.00molN2(g)与3.00molH2(g)混合于一个10.0L密闭容器中,在不同温度下达到平衡时NH3(g)的平衡浓度如图所示.其中温度为T1时平衡混合气体中氨气的体积分数为25.0%.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
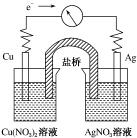 将反应Cu(s)+2Ag+(aq)═Cu2+(aq)+2Ag(s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,下列有关叙述正确的是( )
将反应Cu(s)+2Ag+(aq)═Cu2+(aq)+2Ag(s)设计成原电池,某一时刻的电子流向及电流计(G)指针偏转方向如图所示,下列有关叙述正确的是( )| A. | KNO3盐桥中的K+移向Cu(NO3)2溶液 | |
| B. | Cu作负极,发生还原反应 | |
| C. | 电子由AgNO3溶液通过盐桥移向Cu(NO3)2溶液 | |
| D. | 工作一段时间后,AgNO3溶液中c(Ag+)减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验操作 | 实验现象 | 结论 |
| 打开活塞a,向圆底烧瓶中滴入适量浓盐酸;然后关闭活塞a,点燃酒精灯 | D装置中:溶液变红色;E装置中:水层溶液变黄色,振荡后CCl4层无明显变化 | Cl2、Br2、Fe3+氧化性由强到弱的顺序为Cl2>Br2>Fe3+ |
 ,认为SCN-中碳元素没有被氧化,理由是SCN-中碳元素是最高价态+4价.取D中溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中被氧化的元素是硫元素.通过实验证明了SCN-中氮元素转化为NO3-,若SCN-与Cl2反应生成1mol CO2,则转移电子的物质的量是16mol.
,认为SCN-中碳元素没有被氧化,理由是SCN-中碳元素是最高价态+4价.取D中溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中被氧化的元素是硫元素.通过实验证明了SCN-中氮元素转化为NO3-,若SCN-与Cl2反应生成1mol CO2,则转移电子的物质的量是16mol.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com