
 甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:
甲醇是一种可再生能源,由CO2制备甲醇的过程可能涉及的反应如下:分析 (1)根据盖斯定律:Ⅱ=Ⅰ-Ⅲ得反应②的△H2;
(2)化学反应能否自发进行,取决于焓变和熵变的综合判据,当△G=△H-T•△S<0时,反应能自发进行;
(3)对于可逆反应,化学反应到达平衡时,正逆反应速率相等,各物质的物质的量浓度不再发生变化;
(4)A.温度升高化学反应速率加快,催化剂的催化效率降低;
B.该反应是放热反应,升温平衡逆向移动;
C.反应是放热反应,温度升高平衡逆向进行;
D.温度越低催化剂活性越小,反应速率越慢;
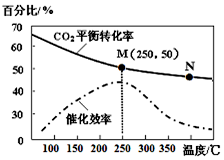
(5)图中M点时二氧化碳的转化率50%,结合化学平衡三行计算列式得到,反应是气体体积减小的反应增大压强平衡正向进行.
解答 解:(1)反应Ⅰ:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1=-49.58kJ•mol-1,反应Ⅱ:CO2(g)+H2(g)?CO(g)+H2O(g)△H2,反应Ⅲ:CO(g)+2H2(g)?CH3OH(g)△H3=-90.77kJ•mol-1,根据盖斯定律:Ⅱ=Ⅰ-Ⅲ得反应②的△H2=+41.19 kJ•mol-1;
故答案为:+41.19 kJ•mol-1;
(2))△G=△H-T•△S<0时,反应能够自发进行,该反应的△S<0、△H<0,当温度较低时,反应Ⅲ能够自发进行,
故答案为:较低温度;
(3)A.由于气体的质量、体积不变,则无论是否达到平衡状态,混合气体的密度都不变化,不能作为判断是否平衡的依据,故A错误;
B.反应前后气体的物质的量不等,混合气体的平均相对分子质量不再变化,可说明气体的物质的量不再变化,说明达到平衡状态,故B正确;
C.平衡常数未知,CO2、H2、CH3OH、H2O的物质的量之比为1:3:1:1,不能判断是否达到平衡状态,故C错误;
D.甲醇的百分含量不再变化,可说明达到平衡状态,故D正确.
故答案为:BD;
(4)A.化学反应速率随温度的升高而加快,催化剂的催化效率降低,所以v(M)有可能小于v(N),故A错误;
B.温度低于250℃时,随温度升高平衡逆向进行甲醇的产率减小,故B错误;
C.升高温度二氧化碳的平衡转化率减低,则升温平衡逆向移动,所以M化学平衡常数大于N,故C正确;
D.为提高CO2的转化率,平衡正向进行,反应是放热反应,低的温度下进行反应,平衡正向进行,但催化剂的活性、反应速率减小,故D错误;
故答案为:ABD;
(5)若在密闭容器中充入体积比为 3:1的 H2 和CO2,设为3mol、1mol,则图中M点时二氧化碳转化率50%,
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始量(mol) 1 3 0 0
变化量(mol) 0.5 1.5 0.5 0.5
平衡量(mol) 0.5 1.5 0.5 0.5
产物甲醇的体积分数=$\frac{0.5}{1.5+0.5+0.5+0.5}$×100%=16.7%,
K=$\frac{0.5×0.5}{0.5×1.{5}^{3}}$=0.148,
反应前后气体体积减小,若要进一步提高甲醇的体积分数,可采取的措施有增大压强平衡正向进行,
故答案为:16.7%;0.148;增大压强.
点评 本题考查较为综合,涉及盖斯定律、化学平衡计算等知识点,为高考常见题型,侧重考查学生图象分析、计算能力,明确化学反应原理是解本题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一有机反应类型 | |
| B. | 单质硅是将太阳能转化为电能的常用材料 | |
| C. | 淀粉、纤维素和油脂都属于天然高分子化合物 | |
| D. | 合成纤维和光导纤维都是新型无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

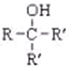
 .写出同时满足下列条件的B的同分异构体的结构简式
.写出同时满足下列条件的B的同分异构体的结构简式 .
. ,该转化中涉及到反应类型为消去反应;该反应的副产物中与D 互为同分异构体的化合物的结构简式为
,该转化中涉及到反应类型为消去反应;该反应的副产物中与D 互为同分异构体的化合物的结构简式为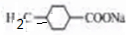 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH=CHCH3分子中的四个碳原子在同一直线上 | |
| B. | 按系统命名法, 的名称为4,4-二甲基-3-乙基己烷 的名称为4,4-二甲基-3-乙基己烷 | |
| C. | 满足分子式为C4H8ClBr的有机物有11种 | |
| D. | 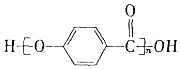 的结构中含有酯基 的结构中含有酯基 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
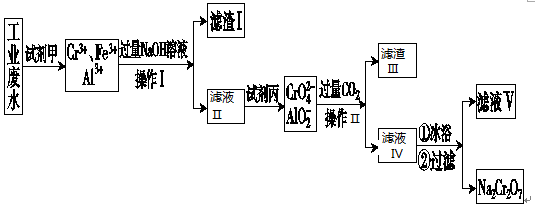
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用物质A表示的反应的平均速率为0.3 mol•L-1•s-1 | |
| B. | 用物质B表示的反应的平均速率为0.6 mol•L-1•s-1 | |
| C. | 2 s 时物质A的转化率为70% | |
| D. | 2 s 时物质B的浓度为1.4 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将1molNH4NO3于稀氨水便溶液呈中性,溶液中NH4+数目为NA | |
| B. | 标准状况下,22.4L甲烷中含有的C-H键数目为3NA | |
| C. | 25℃时,pH=2的硫酸溶液中含有H+的数目为0.01NA | |
| D. | 1molFe与1molCl2充分反应转移电子数为3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com