
����Ŀ���±���Ԫ�����ڱ���һ���֡��������е���ĸ�ֱ����һ�ֻ�ѧԪ�ء�

�Իش��������⣺
��1��I������ϼ�Ϊ__________��K��Ԫ������Ϊ__________��
��2��д����̬ʱQԪ��ԭ�ӵĵ����Ų�ʽ__________��JԪ��ԭ�ӵ���Χ�����Ų�ʽ________________��
��3�����жԱ���ȷ����__________��
a��ԭ�Ӱ뾶H��G��B��A
b����һ������E��D��C��B
c���縺��A��H��G��Q
d������������ˮ��������B��A��H��G
��4�����й���Ԫ����Ԫ�����ڱ��е�λ���Լ�Ԫ��ԭ�ӵ���Χ�����Ų��ص���й���������ȷ����__________��
a��Lλ��Ԫ�����ڱ�����������A�壬����s��Ԫ��
b��Oλ��Ԫ�����ڱ������������壬����ds��Ԫ��
c��M����Χ�����Ų�ʽΪ6s1������ds��Ԫ��
d��H���������Χ�����Ų�ʽΪns2np2������p��Ԫ��
���𰸡� ��6 ͭ 1s22s22p63s23p63d104s24p1 3d64s2 cd bc
�������������������1��I��CrԪ�����۵����Ų���3d54s1��K��29��Ԫ��Cu����2��Q��31��Ԫ��Ga����3�����Ӳ���Խ��뾶Խ���Ӳ�����ͬʱ��������Խ��뾶ԽС��ͬ����Ԫ�ش����ҵ�һ����������NԪ��2p�ܼ�Ϊ�����״̬����һ�����ܴ������ڵ�OԪ�أ�ͬ����Ԫ�ش����ҵ縺����ǿ��ͬ����Ԫ�ش��ϵ��µ縺�Լ�С���ǽ�����Խǿ������������ˮ��������Խǿ����4��L��RbԪ����λ��Ԫ�����ڱ�����������A�壬�۵����Ų���5S1�������Ԫ�أ�����d��Ԫ����M����Χ�����Ų�ʽΪ5d106s1��H�������λ��A������Χ�����Ų�ʽΪns2np2������p��Ԫ����
��������1��I��CrԪ�����۵����Ų���3d54s1����������ϼ�Ϊ+6��K��29��Ԫ��Cu��������ͭ����2��Q��31��Ԫ��Ga����������Ų�ʽ��1s22s22p63s23p63d104s24p1����3�����Ӳ���Խ��뾶Խ���Ӳ�����ͬʱ��������Խ��뾶ԽС��ԭ�Ӱ뾶G��H��A��B����a����ͬ����Ԫ�ش����ҵ�һ����������NԪ��2p�ܼ�Ϊ�����״̬����һ�����ܴ������ڵ�OԪ�أ����Ե�һ������Ne��F��N��O����b����ͬ����Ԫ�ش����ҵ縺����ǿ��ͬ����Ԫ�ش��ϵ��µ縺�Լ�С�����Ե縺��A��H��G��Q����c��ȷ���ǽ�����Խǿ������������ˮ��������Խǿ������������ˮ��������HNO3>H2CO3>H2SiO3>Al(OH)3����d��ȷ����4��L��RbԪ����λ��Ԫ�����ڱ�����������A�壬�۵����Ų���5S1������s��Ԫ������a��ȷ�������Ԫ�أ�����d��Ԫ����Oλ��Ԫ�����ڱ������������壬����d��Ԫ������b������M����Χ�����Ų�ʽΪ5d106s1����c������H�������λ��A������Χ�����Ų�ʽΪns2np2������p��Ԫ������d��ȷ��
�㾦��ͬ����Ԫ�ش����ҵ�һ����������A��Ԫ��p�ܼ�Ϊ�����״̬�������ͣ���һ�����ܴ������ڵ���A��Ԫ�أ���ڶ����ڵ�NԪ�ص�һ�����ܴ���O��
�����͡�������
��������
23
����Ŀ����֪A��B��C��D��E��F��G����Ԫ�����ڱ��ж���������Ԫ�أ����ǵ�ԭ��������������A�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ�D3B�����������Ӿ�����ͬ�ĵ��Ӳ�ṹ��B��C���ɷֱ���A�γ�10�����ӷ��ӣ�B��C��ͬһ���ڣ����߿����γ������ֹ��ۻ����C��F��ͬһ���壬Bԭ��������Ӳ��p�ܼ��ϵĵ��Ӵ��ڰ���״̬��C���������������ڲ��������3����E���������������ڲ��1�����þ����Ԫ�ػش��������⣺
��1��EԪ��ԭ�ӻ�̬�����Ų�ʽ ��
��2���õ����Ų�ͼ��ʾFԪ��ԭ�ӵļ۵��ӹ��� ��
��3��F��GԪ�ض�Ӧ����ۺ����������Խ�ǿ�ķ���ʽΪ ��
��4�����Ӱ뾶D+ B3������һ������B C���縺��C F
������<������>������=������
��5��A��C�γɵ�һ����ɫ������X�й㷺Ӧ�ã�X������A��Cԭ�Ӹ�����1��1��X�ĵ���ʽΪ ����д��Cu��ϡH2SO4��X��Ӧ�Ʊ�����ͭ�����ӷ���ʽ ��
��6��д��E��D������������Ӧ��ˮ���ﷴӦ�Ļ�ѧ����ʽ ��
���𰸡���1��1s22s22p63s23p1��2�֣�
��2��![]() ��2�֣�
��2�֣�
��3��HClO4��2�֣�
��4������1�֣� �� ��1�֣� ����1�֣�
��5��![]() ��2�֣� Cu+2H++H2O2=Cu2++2H2O��2�֣�
��2�֣� Cu+2H++H2O2=Cu2++2H2O��2�֣�
��6��2Al+2NaOH+2H2O=2NaAlO2+3H2����2�֣�
�����������������A�����ڱ���ԭ�Ӱ뾶��С��Ԫ�أ���H��B��N��C��O��D��Na��E��Al��F��S��G��Cl����1��EԪ��ԭ�ӻ�̬�����Ų�ʽ1s22s22p63s23p1���𰸣�1s22s22p63s23p1����2���õ����Ų�ͼ��ʾFԪ�ؼ�SԪ��ԭ�ӵļ۵��ӹ���![]() ���𰸣�
���𰸣�![]() ����F ��GԪ�ض�Ӧ����ۺ�����H2SO4��HClO4�����Խ�ǿ�ķ���ʽΪHClO4���𰸣�HClO4�������Ӳ�ṹ��ͬ�����ӣ�ԭ������Խ��뾶ԽС��Na��<N3�D����һ������N>O��ͬ������ϵ��£��縺�Լ������縺�ԣ�O>S����;��������������H��O�γɵ�H2O2 �ĵ���ʽ��
����F ��GԪ�ض�Ӧ����ۺ�����H2SO4��HClO4�����Խ�ǿ�ķ���ʽΪHClO4���𰸣�HClO4�������Ӳ�ṹ��ͬ�����ӣ�ԭ������Խ��뾶ԽС��Na��<N3�D����һ������N>O��ͬ������ϵ��£��縺�Լ������縺�ԣ�O>S����;��������������H��O�γɵ�H2O2 �ĵ���ʽ��![]() ��Cu��ϡH2SO4��H2O2��Ӧ�Ʊ�����ͭ�����ӷ���ʽ Cu+2H++H2O2=Cu2++2H2O����;
��Cu��ϡH2SO4��H2O2��Ӧ�Ʊ�����ͭ�����ӷ���ʽ Cu+2H++H2O2=Cu2++2H2O����;![]() Cu+2H++H2O2=Cu2++2H2O����E��Al����NaOH��Ӧ�Ļ�ѧ����ʽΪ��2Al+2NaOH+2H2O=2NaAlO2+3H2��
Cu+2H++H2O2=Cu2++2H2O����E��Al����NaOH��Ӧ�Ļ�ѧ����ʽΪ��2Al+2NaOH+2H2O=2NaAlO2+3H2��


 ��ѧ��ʦ����ϵ�д�
��ѧ��ʦ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ԭ��Ӧ�����ֻ�����Ӧ����֮��Ĺ�ϵ��ͼ��ʾ�����л�ѧ��Ӧ������Ӱ���ֵ���
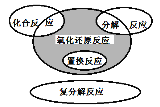
A. Cl2��2NaBr=== 2NaCl2��Br2
B. 4Fe(OH)2��O2��2H2O===4Fe(OH)3
C. 2NaHCO3![]() Na2CO3+CO2��+ H2O
Na2CO3+CO2��+ H2O
D. CH4 + 2O2 ![]() CO2 + 2H2O
CO2 + 2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˼���ij����NaHCO3���ʵ�Na2CO3��Ʒ�Ĵ��ȣ��ֽ�w1 g��Ʒ���ȣ���������Ϊw2 g�������Ʒ��Na2CO3�Ĵ���(��������)��
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л����������������̼���ŷ��йص��ǣ� ��
A.����B.�⻯ѧ����C.�����ն�D.����ЧӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����в���ǰ36��Ԫ�ص����ʻ�ԭ�ӽṹ���±�
Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ |
R | ��̬ԭ�ӵ��������3��δ�ɶԵ��ӣ��������2������ |
S | ��������ˮ���ҷ�Ӧ��������Һ�������� |
T | ��̬ԭ��3d�������1������ |
X | �� |
��1��RԪ�صĵ�һ������Ҫ������ͬ�������ڵ�Ԫ�أ�ԭ����________________________________________________________��
��2��SԪ�صĻ��ϼ��Ƿ������ۣ�__________��ԭ����__________________________________�����������Ų�ʽΪ________________________��
��3��TԪ�ص�ԭ��N�ܲ��ϵ�����Ϊ__________����ԭ�ӽṹʾ��ͼΪ__________��
��4��X�ĺ�������Ų�ͼΥ����__________����X���ʡ�������μ����������εȿ����������ȼ��ʱ�����������ɫ�Ĺ⣬����ԭ�ӽṹ��֪ʶ���ͷ����ԭ��____________________________________________________________________��
���𰸡� ��ԭ��2p���������������ͣ��ȶ� �� F�ĵ縺�����ֻ�ܵõ��� 2s22p5 2 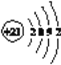 �������ԭ�� ���Ӵ������ϸߵĹ��ԾǨ�������ϵ͵Ĺ��ʱ���Թ����ʽ�ͷ�����
�������ԭ�� ���Ӵ������ϸߵĹ��ԾǨ�������ϵ͵Ĺ��ʱ���Թ����ʽ�ͷ�����
�����������������RԪ�صĻ�̬ԭ���������3��δ�ɶԵ��ӣ��������2�����ӣ�R��NԪ�أ�SԪ�صĵ�������ˮ���ҷ�Ӧ��������Һ�������ԣ�S��FԪ�أ�TԪ�صĻ�̬ԭ��3d�������1�����ӣ�T��21��Ԫ��Sc�� XԪ�ص�ԭ�Ӻ�����12�����ӣ�X��MgԪ�ء�
�������������Ϸ�������1��R��NԪ������ԭ��2p���������������ͣ��ȶ�,���Ե�һ������Ҫ������ͬ�������ڵ�OԪ����
��2��Ԫ��F�ĵ縺�����ֻ�ܵõ���������FԪ��û�����ۣ�FԪ�ص����������Ų�ʽΪ2s22p5��
��3��Scԭ�ӵĺ�������Ų�ʽ��1s22s22p63s23p63d14s2������N�ܲ��ϵ�����Ϊ2����ԭ�ӽṹʾ��ͼΪ ����4�������������ԭ����Mgԭ�������2������Ӧ�Ų���3s����������Ժ�������Ų�ͼΥ�����������ԭ�������Ӵ������ϸߵĹ��ԾǨ�������ϵ͵Ĺ��ʱ���Թ����ʽ�ͷ�����������ȼ�����ʱ�����������ɫ�Ĺ���
����4�������������ԭ����Mgԭ�������2������Ӧ�Ų���3s����������Ժ�������Ų�ͼΥ�����������ԭ�������Ӵ������ϸߵĹ��ԾǨ�������ϵ͵Ĺ��ʱ���Թ����ʽ�ͷ�����������ȼ�����ʱ�����������ɫ�Ĺ���
�����͡�������
��������
20
����Ŀ�����в��ֶ�����Ԫ�ص����ʻ�ԭ�ӽṹ���±���
Ԫ�ر�� | Ԫ�����ʻ�ԭ�ӽṹ |
T | ��������ˮ���ҷ�Ӧ��������Һ�������� |
X | L��p��������s��������2�� |
Y | ��������Ԫ�صļ������а뾶��С |
Z | L��������δ�ɶԵ��� |
��1��д��Ԫ��X�����ӽṹʾ��ͼ__________��
��2��д��YԪ������������ˮ����ֱ���HCl��NaOH��Һ��Ӧ�����ӷ���ʽ_______________________��_________________________��
��3��д��Z��Y�ĵ����Ų�ʽ______________��________________��
��4��Ԫ��T����Ԫ����ȣ��ǽ����Խ�ǿ����__________(��Ԫ�ط��ű�ʾ)�����б�������֤����һ��ʵ����__________��
A����̬�⻯��Ļӷ��Ժ��ȶ���
B�����ʷ����еļ���
C����Ԫ�صĵ縺��
D�������������
E���⻯����X��H���ļ���(X����T��Cl����Ԫ��)
F������������Ȼ���еĴ�����ʽ
��5��̽Ѱ���ʵ����ʲ�������ѧϰ����Ҫ����֮һ��T��X��Y��Z����Ԫ�صĵ����л�ѧ�������Բ�ͬ���������ֵ��ʵ���__________(��Ԫ�ط���)��������________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��һ�ֲ�����ˮ�Ĺ���ǽ������������ͼ�е�ת����ϵ���ش��������⣺
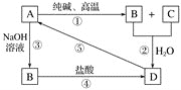
��1��д����ѧʽ��A��____________��D��____________��
��2��д����ط�Ӧ�Ļ�ѧ����ʽ����____________����____________��
��3��д����ط�Ӧ�����ӷ���ʽ����__________����__________����__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ֱ���FeCl3��Һ��������������,�������γɽ�����ǣ� ��
A.ʳ��ˮ
B.��ˮ
C.NaOHŨ��Һ
D.Ũ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ȵĺ������������ClO����ClO��ClO��ClO�ȣ����ڣ����ǵ�˵���в���ȷ����(����)
A. ClO����Cl�ԣ�1�� B. ClO�Ŀռ乹��Ϊֱ����
C. ClO�Ŀռ乹��Ϊ������ D. ClO��SO![]() �ĵȵ�����
�ĵȵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���� 100mL BaCl2��AlCl3 �� FeCl3 �Ļ����Һ A ����μ��� Na2SO4 �� NaOH �Ļ����Һ B�������ij��� �����ʵ���(n)�ͼ�����Һ B �����(V)��ϵ��ͼ��

(1)������ B ��Һ 110mL ʱ����Һ�еij���Ϊ_____(�ѧʽ����ͬ)����Һ�е�������____________________��
(2)�� 90mL �� 100 mL ֮����� 10mL B ��Һʱ���������ӷ�Ӧ����ʽ______��
(3)�� A��B ��Һ�и����ʵ����ʵ���Ũ�������±�
���� | Na2SO4 | NaOH | BaCl2 | AlCl3 | FeCl3 |
c(mol/L) | ___________ | ___________ | ___________ | ___________ | ___________ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com