
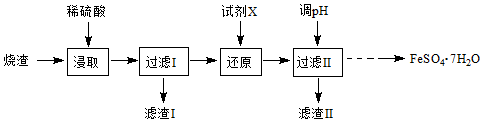
分析 烧渣中加入稀硫酸,得到硫酸铁、硫酸亚铁和硫酸铝,二氧化硅不反应,过滤,滤渣Ⅰ为二氧化硅,在滤液中加入试剂X,还原硫酸铁得到硫酸铝和硫酸亚铁溶液,调节溶液pH,生成氢氧化铝沉淀,滤渣Ⅱ为氢氧化铝,溶液经蒸发结晶、过滤、洗涤、干燥,可得到FeSO4•7H2O,以此解答该题.
解答 解:烧渣中加入稀硫酸,得到硫酸铁、硫酸亚铁和硫酸铝,二氧化硅不反应,过滤,滤渣Ⅰ为二氧化硅,在滤液中加入试剂X,还原硫酸铁得到硫酸铝和硫酸亚铁溶液,调节溶液pH,生成氢氧化铝沉淀,滤渣Ⅱ为氢氧化铝,溶液经蒸发结晶、过滤、洗涤、干燥,可得到FeSO4•7H2O,
(1)二氧化硅不与稀硫酸反应,滤渣1为二氧化硅;
故答案为:SiO2;
(2)试剂X若选用SO2,发生反应:SO2+2Fe3++2H2O=SO42-+2Fe2++4H+,则阴离子为SO42-;
故答案为:SO42-;
(3)滤渣Ⅱ为氢氧化铝,即Al(OH)3,溶液经蒸发浓缩、冷却结晶、过滤、洗涤、干燥,可得到FeSO4•7H2O;
故答案为:蒸发浓缩;冷却结晶;
(4)①配制250mL溶液需要的玻璃仪器除有烧杯、胶头滴管、玻璃棒、250 mL容量瓶;
故答案为:玻璃棒;250 mL容量瓶;
②MnO4-~5Fe2+
25mL溶液中:n(Fe2+)=5 n(MnO4-)=5×0.0100mol/L×20.00×10-3L=10-3 mol,
250 mL溶液中:n(Fe2+)=10-3 mol×10=10-2mol,
1片补血剂样品中:n(Fe2+)=10-3mol,
m(Fe2+)=10-3mol×56g/mol=0.056g=56mg;
故答案为:56.
点评 本题考查化学实验制备方案设计,为高频考点,涉及盐类水解、氧化还原反应等知识点,明确反应原理及物质性质是解本题关键,熟悉流程图中发生的反应及基本操作方法,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ② | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | 芒硝 | NaNO3 |
| B | 熟石膏 | 2CaSO4•H2O |
| C | 明矾 | KAl(SO4)2 |
| D | 绿矾 | FeCl2•7H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓度均为0.2mol•L-1的 Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO32-)+c(HCO3-)] | |
| B. | 浓度相等的a、NH4HSO4溶液、b、NH4HCO3溶液、c、NH4Cl溶液中的c(NH4+):a>b>c | |
| C. | NaHSO3溶液显酸性,c(Na+)>c(HSO3- )>c(H+)>c(OH-)>c(SO32-) | |
| D. | pH=3.6 的0.lmol/LHX 与0.lmol/LNaX 的混合溶液中,2c(H+)-2c(OH-)=c(X-)-c(HX) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冰融化为水的过程△H>0,△S<0 | |
| B. | 在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向 | |
| C. | 在常温下,放热反应一般能自发进行,吸热反应都不能自发进行 | |
| D. | NH4HCO3(s)?NH3(g)+H2O(g)+CO2(g)△H=+185.57kJ/mol,能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 新制氯水中:c(H+)=c(HClO)+2c(ClO-)+c(OH-) | |
| B. | pH=8的NaClO2溶液中:c(Na+)>c(ClO2-)>c(OH-)>c(H+) | |
| C. | 0.1mol•L-1HCl溶液与0.2 mol•L-1 NH3•H2O溶液等体积混合pH>7:c(NH3•H2O)>c(Cl-)>c(NH4+)>c(OH-) | |
| D. | 0.1mol•L-1K2C2O4溶液与0.2 mol•L-1KHC2O4溶液等体积混合:4c(K+)=3[c(C2O42-)+c(HC2O4-)] |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 没有阳光 | B. | 温度太低 | C. | 压强太大 | D. | 缺少CO2和O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com