
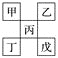
【题目】如下图是从元素周期表中截取下来的,甲、乙、丙为短周期主族元素,下列说法中正确的是( )
A. 丁一定是金属元素,其金属性比丙强
B. 丙的最高价氧化物水化物显强酸性
C. 乙的氢化物是以分子形式存在,且分子间存在氢键
D. 戊的原子序数一定是甲的5倍,且原子半径比甲大
【答案】C
【解析】
甲、乙、丙为短周期主族元素,由位置可知,甲、乙一定为第二周期元素,丙为第三周期元素,丁、戊为第四周期元素,A.丁不一定是金属元素;B.若丙为P元素,则其最高价氧化物对应的水化物不是强酸;C.乙元素可能是N、O、F,则氢化物中含有氢键;D.甲、戊元素不能确定,则原子序数的关系不能确定。
已知甲、乙、丙为短周期主族元素,由图可知甲、乙位于第二周期,丙为与第三周期,丁、戊为第四周期,A.根据元素在周期表中的位置,丁可能是As、Ge、Ga元素,所以丁不一定是金属元素,选项A错误;B.丙元素可能是Si、P、S,若丙为Si、P元素,则其最高价氧化物对应的水化物不是强酸,选项B错误;C.乙元素可能是N、O、F,它们的氢化物均为分子晶体,氢化物中含有氢键,选项C正确;D.甲、戊元素不能确定,则原子序数的关系不能确定,若甲为C元素,则戊为Se元素,不是5倍的关系,选项D错误。答案选C。


科目:高中化学 来源: 题型:
【题目】在生物体内含量极少,但对于维持生物体的正常生命活动必不可少的元素有
A. Fe、Mn、Zn、Mg B. Zn、Cu、Mg、Ca
C. Zn、Cu、B、Mn D. Mg、Mn、Cu、Mo
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机合成中间体的结构简式如右图所示。下列关丁该有机物的叙述正确的是
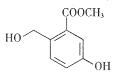
A. 分子式为C9H8O4
B. 在一定条件下可与HCHO发生缩聚反应
C. 在浓硫酸作用下可发生消去反应
D. 1 mol该物质最多能与3mol Br2发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
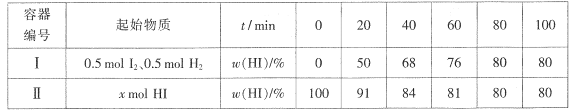
【题目】Boderlscens研究反应:H2(g)+I2(g) ![]() 2HI(g) △H<0.温度T时,在两个体积均为1L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数ω(HI)与反应时间t的关系如下表:
2HI(g) △H<0.温度T时,在两个体积均为1L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数ω(HI)与反应时间t的关系如下表:
研究发现上述反应中![]() 其中
其中![]() 为常数。下列说法正确的是
为常数。下列说法正确的是
A. 温度为T时该反应的![]()
B. 容器I中前20 min的平均速率v(HI)=0.0125mol.L-1.min-1
C. 若起始时,向容器I中加入物质的量均为0.l mol的H2、I2、HI,反应逆向进行
D. 若两容器中![]() 且
且 ![]() 则x的值一定为1
则x的值一定为1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某容器内发生反应N2(g)+3H2(g)![]() 2NH3(g),不可能为平衡状态的是( )
2NH3(g),不可能为平衡状态的是( )
A. NH3、N2、H2的物质的量都不再改变
B. NH3、N2、H2的体积分数都不再改变
C. 混合气体平均相对分子质量不再改变
D. 一个N≡N断裂的同时,有3个H—H键断裂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察如图所示装置,在通电一段时间后,铁电极的质量增加了5.4g. 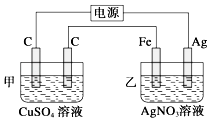
(1)经分析知,甲池是(填“原电池”或“电解池”);乙池中,银电极为极(填“阳极”或“阴极”或“正极”或“负极”).
(2)乙池中银电极的电极方程式为 , 根据题目所示数据,电路中转移了mol 电子.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化物具有不同程度的毒性,会破坏人体的中枢神经,长期吸入会引起脑性麻痹,手脚萎缩等,大量吸入时会引发中枢神经麻痹,记忆丧失,四肢瘫痪,甚至死亡等后果。构成电池方法既能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,发生反应6NO2+8NH3= 7N2+12H2O,装置如图所示。下列关于该电池的说法正确的是 ( )
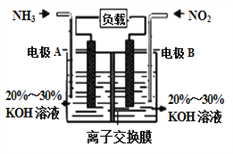
A. 电子从右侧电极经过负载后流向左侧电极
B. 为使电池持续放电,离子交换膜需选用阴离子交换膜
C. 电极A极反应式为2NH3-6e-=N2+6H+
D. 当有4.48LNO2被处理时,转移电子物质的量为0.8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L 恒容密闭容器中,发生反应:X(g)+Y(g)═2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表:下列说法正确的是( )
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2min的平均速率ν(Z)=2.0×10﹣5 mol/(Lmin)
B.4min时,ν(逆)>ν(正)
C.该温度下,此反应的平衡常数K=1.44
D.7min时,反应还未达到平衡状态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com