
| A、向Ba(OH)2溶液中加入过量的NH4HSO4溶液Ba2++2OH-+NH4++H++SO42-═BaSO4↓+NH3?H2O+H2O |
| B、工业上用石灰乳制漂粉精:2OH-+Cl2=Ca2++Cl-+ClO-+H2O |
| C、向漂白粉溶液中通入一定量的SO2Ca2++3ClO-+SO2+H2O=CaSO4+Cl-+2HClO |
| D、向100mL 0.1mol/L NaOH溶液中滴入数滴0.2mol/L Ca(HCO3)2溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O |


科目:高中化学 来源: 题型:
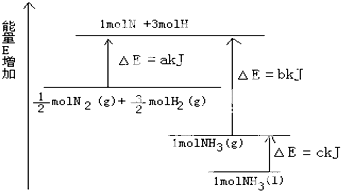 已知化学反应N2+3H2═2NH3的能量变化如图所示:
已知化学反应N2+3H2═2NH3的能量变化如图所示:| 1 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
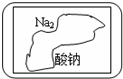 现有一盛有无色固体物质M的试剂瓶,标签已破损(如图).已知硫酸、盐酸、硝酸等是强酸,碳酸、氢硫酸、亚硫酸、醋酸等是弱酸,烧碱、苛性钾等是强碱,一水合氨等是弱碱.由强酸与强碱组成的正盐呈中性,由强酸弱碱组成的正盐呈酸性,由弱酸强碱组成的正盐呈碱性.
现有一盛有无色固体物质M的试剂瓶,标签已破损(如图).已知硫酸、盐酸、硝酸等是强酸,碳酸、氢硫酸、亚硫酸、醋酸等是弱酸,烧碱、苛性钾等是强碱,一水合氨等是弱碱.由强酸与强碱组成的正盐呈中性,由强酸弱碱组成的正盐呈酸性,由弱酸强碱组成的正盐呈碱性.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子总数 | B、密度 |
| C、质量 | D、质子总数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔既是表示微粒,又是表示质量的单位 |
| B、1mol氧的质量等于16g |
| C、氢氧化钠的摩尔质量是40g |
| D、氩气的摩尔质量(以g/molWei单位)在数值上等于它的相对原子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ |
| B、Na2O2与H2O反应制备O2:Na2O2+H2O═2Na++2OH-+O2↑ |
| C、将氯气溶于水制备次氯酸:Cl2+H2O═2H++Cl-+ClO- |
| D、用酸性KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++7H2O2═2Mn2++6O2↑+10H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
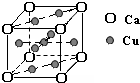 【物质结构域性质】
【物质结构域性质】查看答案和解析>>
科目:高中化学 来源: 题型:
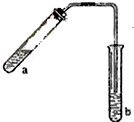 哈三中某化学课外学习小组利用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去).请填空:
哈三中某化学课外学习小组利用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去).请填空:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com