
| A. | 把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 | |
| B. | 用锌片做阳极,铁片做做阴极,电解氯化锌溶液,铁片表面出现一层锌 | |
| C. | 把要保护的金属与直流电负极相连,这种方法叫牺牲阳极的阴极保护法 | |
| D. | 把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
分析 A.铜片和铁片和稀硫酸构成原电池,铜作正极;
B.阳极是活性金属锌,所以阳极金属锌失去电子发生氧化反应,阴极上溶液中的阳离子即锌离子得到电子变成锌,在铁极上析出;
C.外加电流保护金属称为外加电流的阴极保护法;
D.构成原电池反应,可以加速反应的速率.
解答 解:A.把铜片和铁片紧靠在一起浸入稀硫酸中,形成铜、铁、稀硫酸原电池,正极是金属铜,该极上电子和溶液中的氢离子结合产生氢气,故A正确;
B.用锌片做阳极,铁片做做阴极,电解氯化锌溶液,这是一个电镀池,镀层金属锌作阳极,待镀件铁作阴极,镀层金属盐氯化锌溶液作电解质,发生反应:阳极:Zn-2e-=Zn2+;阴极:Zn2++2e-=Zn,故B正确;
C.被保护金属与直流电源的负极相连时,是外加电流的阴极保护法,故C错误;
D.把锌片放入盛盐酸的试管中,加入几滴氯化铜溶液,锌置换出铜,所以形成了铜、锌、稀盐酸原电池,原电池反应可以加速反应的速率,故D正确;
故选C.
点评 本题主要考查了原电池的有关应用,解答须理解原电池的构成条件反应原理,题目较简单.


科目:高中化学 来源: 题型:解答题
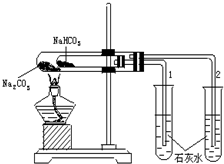 实验室利用如图所示装置进行Na2CO3和NaHCO3热稳定性对比实验.请回答:
实验室利用如图所示装置进行Na2CO3和NaHCO3热稳定性对比实验.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 为原料(其它无机试剂任选),合成
为原料(其它无机试剂任选),合成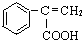 的流程图如下.请回答:
的流程图如下.请回答: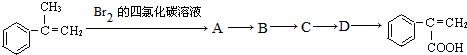
 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖尿病患者不宜食用含糖量高的食物 | |
| B. | 人体如果摄入的糖类过多,它在体内转化为多余的脂肪,引起肥胖 | |
| C. | 如果人在较长时间内未进食,人体就无法摄取能量 | |
| D. | 人体摄入的蛋白质,在酶的作用下水解,最终生成氨基酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 放电时,CH3OH参与反应的电极为正极 | |
| B. | 放电时,负极反应为:CH3OH-6e-+8OH-═CO32-+6H2O | |
| C. | 充电时,电解质溶液的pH逐渐增大 | |
| D. | 放电时,每通入标况下11.2L O2完全反应转移电子数为1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某温度时在2L容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:
某温度时在2L容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据分析:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+、Cl-、NO3-、Na+ | B. | Na+、K+、NH4+、Ba2+ | ||
| C. | Na+、S2-、Cl-、CO32- | D. | K+、NO3-、SO42-、HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com