
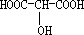 ;
;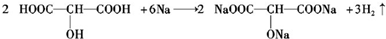 ;
;分析 由①可知,Mr(A)=60×2=120.由②可知,n(CO2)=$\frac{3.36L}{22.4L/mol}$=0.15mol,n(H2O)=$\frac{1.8g}{18g/mol}$=0.1mol,A中含n(O)=$\frac{6g-0.15mol×12g/mol-0.2mol×1g/mol}{16g/mol}$=0.25mol,则A分子中C、H、O的原子个数比为0.15mol:0.2mol:0.25mol=3:4:5,最简式为C3H4O5,最简式相对分子质量为120,与A的相对分子质量相等,故A的分子式为C3H4O5.③1mol物质A发生酯化反应,转化完全时消耗乙醇92g,乙醇物质的量为$\frac{92g}{46g/mol}$=2mol,则A分子中含2个-COOH,1molA能与足量的金属钠反应放出33.6L氢气(标准状况),氢气为$\frac{33.6L}{22.4L/mol}$=1.5mol,2mol羧基得到1mol氢气,故A分子中还含有1个-OH,则A的结构简式为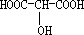 ,据此解答.
,据此解答.
解答 解:由①可知,Mr(A)=60×2=120.由②可知,n(CO2)=$\frac{3.36L}{22.4L/mol}$=0.15mol,n(H2O)=$\frac{1.8g}{18g/mol}$=0.1mol,A中含n(O)=$\frac{6g-0.15mol×12g/mol-0.2mol×1g/mol}{16g/mol}$=0.25mol,则A分子中C、H、O的原子个数比为0.15mol:0.2mol:0.25mol=3:4:5,最简式为C3H4O5,最简式相对分子质量为120,与A的相对分子质量相等,故A的分子式为C3H4O5.③1mol物质A发生酯化反应,转化完全时消耗乙醇92g,乙醇物质的量为$\frac{92g}{46g/mol}$=2mol,则A分子中含2个-COOH,1molA能与足量的金属钠反应放出33.6L氢气(标准状况),氢气为$\frac{33.6L}{22.4L/mol}$=1.5mol,2mol羧基得到1mol氢气,故A分子中还含有1个-OH,则A的结构简式为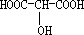 .
.
(1)由上述分析可知,A的实验式为C3H4O5,结构简式为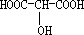 ,故答案为:C3H4O5;
,故答案为:C3H4O5;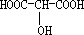 ;
;
(2)A与足量的钠反应的化学方程式为: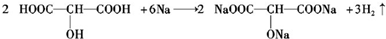 ,
,
故答案为: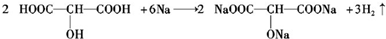 ;
;
(3)某物质B与A互为同系物,分子中只相差一个CH2的同分异构体有: ,
,
故答案为:3.
点评 本题考查有机物推断,利用守恒法得出最简式,再根据发生的反应确定官能团种类及数目,题目难度中等.


 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:选择题
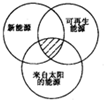
| A. | 煤炭、石油、潮汐能 | B. | 水能、生物质能、天然气 | ||
| C. | 太阳能、风能、生物质能 | D. | 地热能、海洋能、核能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
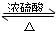 CH3COOC2H5+H2O,该反应的反应类型为取代或酯化反应.
CH3COOC2H5+H2O,该反应的反应类型为取代或酯化反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①溶液逐渐变红色的原因是Fe2+被酸性KMnO4溶液氧化 | |
| B. | ②红色逐渐褪去的原因是酸性KMnO4溶液将SCN-氧化 | |
| C. | ②红色逐渐褪去的原因是酸性KMnO4溶液将Cl-氧化 | |
| D. | ③溶液又逐渐变色且为紫色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 常温下,1.8g H2O含有0.2nA个H-O共价键 | |
| B. | 1L 0.3 mol•L-1的FeCl3溶液中Fe3+数目为0.3nA | |
| C. | 标准状况下,22.4L CCl4中含 nA个CCl4分子 | |
| D. | 标准状况下,22.4L NO2和CO2的混合气体含有2nA个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2 | B. | CH3CH=CH2 | C. | CH3CH3 | D. | CH3CH2CH=CH2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com