
【题目】下列说法正确的是
A.金属单质在反应中只能作还原剂,非金属单质只能作氧化剂
B.失电子多的金属还原性强
C.某元素从化合态到游离态,该元素一定被还原
D.金属阳离子被还原不一定得到金属单质
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如果将前18号元素按原子序数递增的顺序排列,可形成如图所示的“蜗牛”形状,图中每个“![]() ”代表一种元素,其中
”代表一种元素,其中![]() 点代表氢元素
点代表氢元素![]() 下列说法不正确的是( )
下列说法不正确的是( )

A. 最高价氧化物对应水化物的酸性![]() 比
比![]() 弱
弱
B. 最简单气态氢化物的稳定性![]() 比
比![]() 小
小
C. 金属性![]() 比
比![]() 弱
弱
D. 原子半径![]() 比
比![]() 大
大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硝酸银溶液为滴定液,测定能与Ag+反应生成难溶性电解质的一种容量分析方法叫银量法。其原理如下:
①Ag++X-=AgX↓(X-表示Cl-、Br-、I-、CN-、SCN-等离子)——用于定量计算
②2Ag++CrO42-=Ag2CrO4↓(砖红色)——用于指示滴定的終点
[已知: Ksp(AgCl)=2.0×10-10,Ksp(Ag2CrO4)=1.12×10-12]。
某氯碱厂为测定饱和食盐水被电解后所得淡盐水(见图)里氯化钠的浓度,采用以上银量法,每次取20.00ml 淡盐水进行滴定,共进行了三次。据此,回答下列问题:

(1)配制100mL 0.4mol/L的硝酸银溶液(标准液)时,需要用托盘天平称取____gAgNO3固体,制成的溶液需置于棕色试剂瓶中(备用),原因是_______________。
(2)为了使溶液中的Cl-恰好沉淀完全(溶液中残余Cl-的浓度是1.0×10-5mol/L),溶液中(CrO42-)的浓度度应为______mol/L,若CrO42-的浓度大于此数值,则测定结果会偏_____(填“高”或“低”)。滴定时,若此时消耗AgNO3溶液25.00mL.( 三次实验的平均值),则淡盐水中氯化钠的浓度是______mol/L。
(3)根据相关离子的性质,滴定时溶液的pH值应控制在6.5~10,pH值太大或太小对实验均有不良影响,pH值太大的不良影响是__________(用离子反应方程式表示)。
(4)AgCl沉淀易吸附Cl-为减少AgC1沉淀对Cl-的吸附,从而减小实验的误差,实验时应采取的措施是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在初始温度为500℃、容积恒定为10L的三个密闭容器中,如图充料发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H=-25kJ/mol。已知乙达到平衡时气体的压强为开始时的0.55倍;乙、丙中初始反应方向不同,平衡后对应各组分的体积分数相等。下列分析正确的是( )
CH3OH(g)+H2O(g)△H=-25kJ/mol。已知乙达到平衡时气体的压强为开始时的0.55倍;乙、丙中初始反应方向不同,平衡后对应各组分的体积分数相等。下列分析正确的是( )
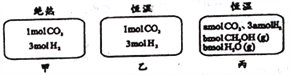
A. 刚开始反应时速率:甲>乙 B. 平衡后反应放热:甲>乙
C. 500℃下该反应平衡常数:K=3×102 D. 若a≠0,则0.9<b<l
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关键能数据如表:
化学键 | Si﹣O | O=O | Si﹣Si |
键能/kJmol﹣1 | X | 498.8 | 176 |
晶体硅的燃烧热为989.2kJmol﹣1 , 则X的值为( )
A.423.3
B.460
C.832
D.920
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上),戊、己分别是空气、地壳中含量最多的元素。下列判断正确的是

A. 甲一定是金属元素
B. 气态氢化物的稳定性:庚>己>戊
C. 乙、丙、丁的最高价氧化物水化物可以以相互反应
D. 庚的最高价氧化物水化物酸性最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下事实不能用元素周期律解释的是
A. F2在暗处遇H2即爆炸,I2在暗处遇H2几乎不反应
B. “NO2球”在冷水中颜色变浅,在热水中颜色加深
C. 氯原子与钠原子形成离子键,与硅原子形成共价键
D. H2O在4000℃以上开始明显分解,H2S用酒精灯加热即可完全分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿矾的化学式可表示为FeSO4·xH2O,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的某些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加少量稀H2SO4后,再滴加KSCN溶液,溶液颜色无明显变化。充分振荡后,溶液逐渐变红。溶液变红的原因是_________(用离子方程式表示)。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1 g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按下图连接好装置进行实验。

①下列实验操作步骤的正确排序为___________________(填标号);重复上述操作步骤,直至A恒重,记为m3g。
a.关闭K1和K2 b.打开K1和K2,缓缓通入N2 c.点燃酒精灯,加热 d.称量A e.冷却到室温 f.熄灭酒精灯
②判断A是否恒重的方法是____________________。
③根据实验记录,绿矾化学式中结晶水数目x=________________(列式表示)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入由下图所示仪器组装而成的装置中,打开K1和K2,缓缓通入N2一段时间后,加热。实验后反应管中残留固体为红色粉末。
①反应中有两种气体产物生成,为检验该气体混合物的组成,请从下图所示的仪器中,选择合适的仪器(含其中的试剂),组成一套实验装置,该装置的连接顺序(按气体流向从左到右)依次为___________→D(填装置序号)。装置中除有气泡冒出外,其他证明实验结论的现象分别为__________________________。

②硫酸亚铁高温分解的化学方程式为_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com