
| ���� | K2Cr2O7��Һ | Cr��OH��3 | Cr3+��Һ |
| ��ɫ | �Ȼ�ɫ | ����ɫ���� | ����ɫ |
| Fe��OH��3 | Cr��OH��3 | |
| ��ʼ����ʱ | 1.5 | 6.0 |
| ������ȫʱ | 2.8 | 8.0 |
| ʵ�� ��� | ʵ��װ�� | ʵ���ѹ | ��Һ | ʱ�� | ���� |
| �� |  | 22V | 0.01mol/L K2Cr2O7��Һ | 20 ���� | a �������������� b ��������ɫ���ݣ� |
| ʵ�� ��� | ʵ��װ�� | ʵ���ѹ | ��Һ | ʱ�� | ���� |
| �� |  | 22V | 0.01mol/LK2Cr2O7��Һ�м�������H2SO4�� ����ʹpH��1 | 20 ���� | a ������Һ��dz��ɫ�� b��������ɫ���ݲ������������ɫ������ |
���� ��1��FeSO4���л�ԭ�ԣ�����Cr2O72-+����������ԭ��Ӧ����Fe3+��Cr3+��
��2��Cr3+��Һ�м���NaOH����Cr��OH��3������
��3��Fe������ʧ���������������ӣ�����������K2Cr2O7��Ӧ�������������������軯����Һ��
��4��������Feʧ���������������ӣ������������ӵõ�������������Fe2+��Cr2O72-������Fe3+��Fe3+�������ƶ������������ӽ�ϣ�
��5�����������£�Cr2O72-����ǿ�����ԣ�
��6��pH=8ʱ��Cr3+ת��ΪCr��OH��3������
��� �⣺��1��FeSO4���л�ԭ�ԣ�����Cr2O72-+����������ԭ��Ӧ����Fe3+��Cr3+����Ӧ�����ӷ���ʽΪCr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O��
�ʴ�Ϊ��1��6��1��4��2��6��7��
��2��Cr3+��Һ�м���NaOH����Cr��OH��3�������䷴Ӧ�����ӷ���ʽΪ��Cr3++3OH-=Cr��OH��3����
�ʴ�Ϊ��Cr3++3OH-=Cr��OH��3����
��3�����õ�ⷨ����Fe2+��Fe2+��K2Cr2O7��ԭ��Cr3+����Fe������ʧ���������������ӣ�����Fe����������a��ΪFe�������������������軯����Һ������Ϊȡa ����������Һ���Թ��У������еμ����軯����Һ������ɫ����������˵�������������ӣ�
�ʴ�Ϊ��Fe��ȡa ����������Һ���Թ��У������еμ����軯����Һ������ɫ����������
��4��a��Ϊ������������Feʧ���������������ӣ�����a ������Һ��dz��ɫ��b��Ϊ�����������������ӵõ�����������������b��������ɫ���ݲ�����a��������Fe2+��Cr2O72-������Fe3+��Fe3+Ǩ�Ƶ�b��������OH-�������Fe��OH��3������b�����к��ɫ�������ɣ�
�ʴ�Ϊ����Һ��dz��ɫ������ɫ���������a��������Fe2+��Cr2O72-������Fe3+��Fe3+Ǩ�Ƶ�b��������OH-�������Fe��OH��3��
��5��ʵ����ʵ���������Ż����Ա�ʵ���֪��ʵ��II�ڼ�����һ���������ᣬ��Һ������ǿ�����������£�Cr2O72-����ǿ�����ԣ�
�ʴ�Ϊ��������ҺpHΪ���ԣ���֤Cr2O72-�������ԣ�
��6��pH=8ʱ��Cr3+ת��ΪCr��OH��3����������Ҫ���ڵ������н�Cr2O72-ת��ΪCr��OH��3������ȥ����Ҫ������Һ��pH��
�ʴ�Ϊ��������ҺpH��������Χ ʹCr2O72-��Fe2+������Ӧ��Cr��OH��3�ܳ�����
���� ���⿼���˵��ԭ����Ӧ�á�������ԭ��Ӧ�����ʵ�ת������Ŀ�Ѷ��еȣ�ע����յ������������Ϸ����ķ�Ӧ�Լ�Ԫ�ػ���������ʣ������ڿ���ѧ���ķ��������ͶԻ���֪ʶ��Ӧ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| I1/kJ•mol-1 | I2/kJ•mol-1 | I3/kJ•mol-1 | I4/kJ•mol-1 | I5/kJ•mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�������и�һ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��״���£�aL����X2��bL����Y2ǡ����ȫ��Ӧ����cL����Z����2a=6b=3c����Z�Ļ�ѧʽΪ
A��X3Y B��XY3 C��XY2 D��X2Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������������ʯȼ�� | |
| B�� | ��ҵ������ˮ�����������ŷ� | |
| C�� | ũ����ոѵ�¶������Ʒ��� | |
| D�� | ���������ϡ�������ֽ�����ƷӦ������մ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��CaCl2��Һ��ͨ��������CO2��Ca2++CO2+H2O�TCaCO3��+2H+ | |
| B�� | ��̼�������Һ�м����������������Һ��HCO3-+OH-�TCO32-+H2O | |
| C�� | ��Cu���м��������ŨHNO3��Cu+4H++2NO3-�TCu2++2NO2��+2H2O | |
| D�� | �Ȼ����Һ�����Ե�ԭ��NH4++OH-=NH3•H2O+H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
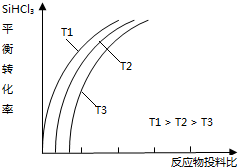 ����Ԫ�صĻ�����㷺��������Ȼ���У����������ﹲͬ������ʯ������裨�۵� 1410�棩��;�㷺����ȡ���ᴿ�����ж��֣�
����Ԫ�صĻ�����㷺��������Ȼ���У����������ﹲͬ������ʯ������裨�۵� 1410�棩��;�㷺����ȡ���ᴿ�����ж��֣��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
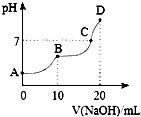 25��ʱ����10mL 0.1mol•L-1 H2C2O4��Һ�еμӵ�Ũ�ȵ�NaOH��Һ����Һ��pH��NaOH��Һ�������ϵ��ͼ��ʾ��������������ȷ���ǣ�������
25��ʱ����10mL 0.1mol•L-1 H2C2O4��Һ�еμӵ�Ũ�ȵ�NaOH��Һ����Һ��pH��NaOH��Һ�������ϵ��ͼ��ʾ��������������ȷ���ǣ�������| A�� | C����Һ�к���NaHC2O4��Na2C2O4 | |
| B�� | NaHC2O4��Һ��ˮ�ĵ���̶ȱ�Na2C2O4��Һ��С | |
| C�� | B�㣬c ��Na+��=2[c ��H2C2O4��+c ��HC2O4-��+c ��C2O42-��] | |
| D�� | D�㣬c ��Na+����c ��C2O42-����c ��OH-����c ��HC2O4-����c ��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��������ƽ��ȡ8.84gʳ�� | |
| B�� | ��250mL����ƿ���������220mL��0.1mol•L1��NaOH��Һ | |
| C�� | ����Ͳ��ȡ12.12mL������ | |
| D�� | ��0.02mol•L-1����ζ�δ֪Ũ�ȵ�NaOH��Һ����������21.00mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���㽭ʡ��һ�ϵ�һ���ʼ컯ѧ���������棩 ���ͣ�ѡ����
���е��뷽��ʽ�������
A��CaCl2 = Ca2++2Cl- B��Na2SO4=2Na+ +SO42-
C��HNO3=H++NO3- D��KClO3=K++C1-+3O2-
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com