
【题目】N2O俗称“笑气”,曾用作可吸入性麻醉剂。以下反应能产生N2O:3CO+2NO2![]() 3CO2+N2O。下列关于N2O的说法正确的是( )
3CO2+N2O。下列关于N2O的说法正确的是( )
A. 上述反应中每生成1 mol N2O,转移的电子数为3NA
B. 等物质的量的N2O和CO2含有相等的电子数
C. N2O只具有氧化性,无还原性
D. N2O会迅速与人体血红蛋白结合,使人中毒
【答案】B
【解析】
A、由方程式3CO+2NO2═3CO2+N2O可知,生成lmolN2O,需要3molCO,物质的量一定,影响气体的体积因素有温度、压强等,CO的状态不一定是标准状况;B、N2O和CO2每个分子都含有22个电子,物质的量相同含有的电子数相同;C、N2O中N元素化合价为+1价,氮元素的化合价常用中间价态,化合价可以升高,也可以降低;D、NO会迅速与人体血红蛋白结合,使人中毒。
A、由方程式3CO+2NO2═3CO2+N2O可知,生成lmolN2O,需要3molCO,物质的量一定,影响气体的体积因素有温度、压强等,CO的状态不一定是标准状况,消耗CO的体积不一定是67.2L,选项A错误;B、N2O和CO2每个分子都含有22个电子,物质的量相同含有的电子数相同,选项B正确;C、N2O中N元素化合价为+1价,氮元素的化合价常用中间价态,化合价可以升高,也可以降低,N2O既有氧化性,又有还原性,选项C错误;D、一氧化二氮不会与血红蛋白结合,可以与人体血红蛋白结合、使人中毒的氮的氧化物是NO,选项D错误。答案选B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知苯乙烯(b)、立方烷(d)、环辛四烯(p)的分子式均为C8H8。下列说法正确的是

A. b、d的二氯代物均只有三种 B. b、p均能与酸性高锰酸钾溶液反应
C. d是烷烃,只能取代,不能加成 D. b和苯乙炔一样,所有原子一定处于同一平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中利用CoCl2·6H2O为原料制取三氯化六氨合钴[Co(NH3)6Cl3]的实验步骤如下:
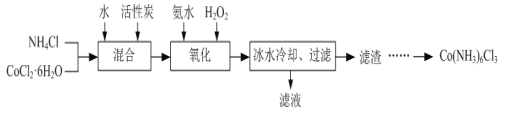
已知:①Co(NH3)6Cl3在不同温度下水中的溶解度曲线如图。
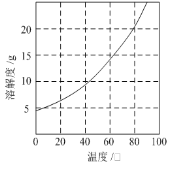
②在Co(NH3)6Cl3溶液中加入一定量盐酸有利于结晶。
③Ksp[Co(OH)2]=1.09×10-15,Ksp[Co(OH)3]=2×10-44。
(1)在实验过程中NH4Cl除作反应物外,还可防止在滴加氨水时c(OH-)过大,其原理是______。
(2)氧化过程中加入氨水和H2O2在溶液中生成Co(NH3)6Cl3。
①氧化时须先加入氨水再加入H2O2,其原因是______。
②该反应的化学方程式为______。
③反应时需要控制反应温度在50 ℃~60 ℃之间,可采取的加热方式是______。
(3)冰水冷却的目的是______。
(4)请补充完整由过滤后所得滤渣获取Co(NH3)6Cl3的实验方案:将滤渣加入沸水中,充分搅拌,______,低温干燥。(实验中须使用的试剂:盐酸、乙醇)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组研究铝土矿中Al2O3的含量。查阅资料得知,铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:

(1)第①步,向铝土矿中加入足量烧碱溶液,充分反应,发生反应的离子方程式是:______________ 、________________;
(2)第③步中,生成氢氧化铝的离子方程式是_____________。若往A溶液中通入足量CO2,产生的沉淀为____________________(填化学式);
(3)工业上制取AlCl3常用Al2O3与C、Cl2在高温条件下反应,已知每消耗0.5mol碳单质,转移1mol电子,则该反应的氧化产物为_____________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列数据中合理的是( )
A.用10 mL量筒量取7.13 mL稀盐酸
B.用托盘天平称量25.20 g NaCl
C.用广范pH试纸测得某溶液的pH为2.3
D.用温度计测量某溶液温度为20.2℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某容器中发生一个化学反应,反应过程中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种离子.在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示.下列有关判断中不正确的是( )
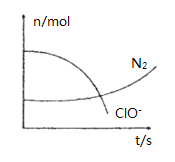
A. 还原剂是含CN-的物质,氧化产物只有N2
B. 氧化剂是ClO-,HCO3-是氧化产物
C. 参与反应的氧化剂与还原剂的物质的量之比为5:2
D. 标准状况下若生成2.24LN2,则转移电子1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄酒中抗氧化剂的残留量是以游离SO2的含量计算,我国国家标准(CB2760-2014)规定葡萄酒中SO2的残留量≤0.25g/L。某兴趣小组设计实验方案对葡萄酒中SO2进行测定。
I.定性实验方案如下:
(1))利用SO2的漂白性检测干白葡萄酒(液体为无色)中的SO2或H2SO3。设计如下实验:

实验结论:干白葡萄酒不能使品红溶液褪色,原因是:___________。
II.定量实验方案如下(部分装置和操作略):

(2)A中加入100.0mL葡萄酒和适量盐酸,加热使SO2全部逸出并与B中H2O2完全反应,其化学方程式为________________。
(3)除去B中过量的H2O2,然后再用NaOH标准溶液进行滴定,除去H2O2的方法是_______。
(4)步骤X滴定至终点时,消耗NaOH溶液30.00mL,该葡萄酒中SO2的含量为_____g/L。该测定结果比实际值偏高,分析原因__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com