


科目:高中化学 来源: 题型:
| 实验步骤 | 实验结论 |
| ①氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 | 氧化性从强到弱的顺序:氯、溴、碘 |
| ②NaBr溶液+氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 | |
| ③KI溶液+氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、②①③ |
| C、③②① | D、①③② |
查看答案和解析>>
科目:高中化学 来源: 题型:
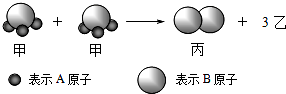 如图所示2个甲分子反应生成1个丙分子和3个乙分子,下列判断不正确的是( )
如图所示2个甲分子反应生成1个丙分子和3个乙分子,下列判断不正确的是( )| A、1个乙分子中含有2个A原子 |
| B、该反应类型是分解反应 |
| C、该反应一定属于氧化还原反应 |
| D、摩尔质量关系为:2M (甲)=M (乙)+M (丙) |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.6 g CH4中含有的电子数 |
| B、100 mL 1 mol/L H2SO4中含有的H+数 |
| C、24 g Mg与足量稀盐酸反应转移的电子数 |
| D、标准状况下,22.4 L CO气体中含有的原子数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com