
某种粗盐中含有泥沙、Ca2+、Mg2+、Fe3+、SO等杂质。某同学在实验室中设计了用这种粗盐制备精盐的方案如下(用于沉淀的试剂稍过量):

请回答以下问题:
(1)为操作Ⅳ选择所需仪器(用标号字母填写):________。
A.烧杯 B.试管 C.玻璃棒 D.分液漏斗 E.漏斗 F.酒精灯
G.蒸发皿
(2)操作Ⅲ中常用Na2CO3溶液、NaOH溶液、BaCl2溶液作为除杂试剂,则加入除杂试剂的顺序为:NaOH溶液→________→________。
(3)操作Ⅲ中,判断加入BaCl2已过量的方法是___________________________________
(4)操作Ⅴ应选择的酸是________,若将操作Ⅴ与操作Ⅳ的先后顺序对调,将会对实验结果产生的影响是___________________________________
(5)操作Ⅵ是________(选择合理操作的名称,用标号字母按操作先后顺序填写)。
a.过滤、洗涤 B.蒸发、浓缩 c.萃取、分液 D.冷却、结晶
(1)ACE (2)BaCl2溶液 Na2CO3溶液
(3)取所得溶液的上层清液于试管中,再滴入少量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量 (4)盐酸 在酸性条件下,会有部分沉淀溶解,从而影响精盐的纯度 (5)bda
【解析】(1)操作Ⅳ是过滤。(2)除杂试剂是过量的,为了除去过量的Ba2+,需要在加入BaCl2溶液之后加入Na2CO3溶液。(3)BaCl2过量后,溶液中不存在SO42— ,取上层清液加入BaCl2溶液后不会产生沉淀。(4)加入的Na2CO3溶液是过量的,加入盐酸调节溶液的pH即可除去CO32—,得到纯净的食盐水。若在过滤前酸化,则在酸性条件下,会有部分沉淀溶解,从而影响精盐的纯度。(5)从食盐水得到食盐晶体需要经过蒸发、浓缩、冷却、结晶、过滤、洗涤等过程。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2013-2014学年高考化学二轮复习四川配套训练 第6讲反应速率和化学平衡练习卷(解析版) 题型:填空题
向一容积不变的密闭容器中充入一定量A和B,发生反应:xA(g)+2B(s) yC(g) ΔH<0。在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示。请回答下列问题:
yC(g) ΔH<0。在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示。请回答下列问题:

(1)用A的浓度变化表示该反应0~10 min内的平均反应速率v(A)=________。
(2)根据图示可确定x∶y=________。
(3)0~10 min容器内压强________(填“变大”、“不变”或“变小”)。
(4)推测第10 min引起曲线变化的反应条件可能是________;第16 min引起曲线变化的反应条件可能是________。
①减压 ②增大A的浓度 ③增大C的量 ④升温
⑤降温 ⑥加催化剂
(5)若平衡Ⅰ的平衡常数为K1,平衡Ⅱ的平衡常数为K2,则K1________K2(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习四川配套训练 第2讲化学常用计量练习卷(解析版) 题型:填空题
工业上用含锌物料(含FeO、CuO等杂质)可制得活性ZnO,流程如下:

(1)上述流程中,浸出用的是60%H2SO4(1.5 g·cm-3),配制这种H2SO4 100 mL需要18.4 mol·L-1的浓H2SO4________ mL(保留一位小数)。
(2)加入氧化剂H2O2后,有Fe(OH)3沉淀出现,没有Cu(OH)2沉淀出现,若溶液中c(Fe3+)=2.6×10-18 mol·L-1,则溶液中c(Cu2+)的取值范围是________mol·L-1。(已知Ksp[Fe(OH)3]=2.6×10-39,
Ksp[Cu(OH)2]=2.2×10-20)
(3)加入NH4HCO3后生成的沉淀是形态均为Zna(OH)b(CO3)c(a、b、c为正整数)的两种碱式碳酸锌A和B的混合物,A中a=5、b=6,则生成碱式碳酸锌A的化学方程式为__________________________________________________。
(4)取洗涤、烘干后的碱式碳酸锌A和B的混合物49.70 g,其物质的量为0.10 mol,高温焙烧完全分解得到37.26 g ZnO、3.584 L CO2(标准状况下)和水,通过计算求出碱式碳酸锌B的化学式。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习四川配套训练 第1讲物质组成性质分类练习卷(解析版) 题型:选择题
下列说法正确的是( )。
A.蛋白质在氧气中完全燃烧转化为水和二氧化碳
B.淀粉和纤维素的分子式均可表示成(C6H10O5)n,它们互为同分异构体
C.与碱反应生成盐和水的氧化物均为酸性氧化物
D.离子化合物中可能含有共价键
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习四川配套训练 第13讲实验方案的设计练习卷(解析版) 题型:实验题
某酸性工业废水中含有K2Cr2O7。光照下,草酸(H2C2O4)能将其中的Cr2O72—转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)在25 ℃下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,做对比实验,完成以下实验设计表(表中不要留空格)。
实验编号 | 初始pH | 废水样品体积/mL | 草酸溶液体积/mL | 蒸馏水体积/mL |
① | 4 | 60 | 10 | 30 |
② | 5 | 60 | 10 | 30 |
③ | 5 | 60 |
|
|

测得实验①和②溶液中的Cr2O72—浓度随时间变化关系如图所示。
(2)上述反应后草酸被氧化为________(填化学式)。
(3)实验①和②的结果表明________;实验①中0~t1时间段反应速率v(Cr3+)=________mol·L-1·min-1(用代数式表示)。
(4)该课题组对铁明矾[Al2Fe(SO4)4·24H2O]中起催化作用的成分提出如下假设,请你完成假设二和假设三:
假设一:Fe2+起催化作用:
假设二:________;
假设三:________;
……
(5)请你设计实验验证上述假设一,完成下表中内容。
(除了上述实验提供的试剂外,可供选择的药品有K2SO4、FeSO4、K2SO4·Al2(SO4)3·24H2O、Al2(SO4)3等。溶液中Cr2O72—的浓度可用仪器测定)
实验方案(不要求写具体操作过程) | 预期实验结果和结论 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习四川配套训练 第11讲有机化学基础练习卷(解析版) 题型:填空题
某课题组以苯为主要原料,采用以下路线合成利胆药——柳胺酚
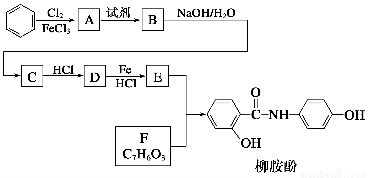
已知:
回答下列问题:
(1)对于柳胺酚,下列说法正确的是________。
A.1 mol柳胺酚最多可以和2 mol NaOH反应
B.不发生硝化反应
C.可发生水解反应
D.可与溴发生取代反应
(2)写出A→B反应所需的试剂________。
(3)写出B→C的化学方程式________________________________。
(4)写出化合物F的结构简式__________。
(5)写出同时符合下列条件的F的同分异构体的结构简式________________
________________________________________(写出3种)。
①属酚类化合物,且苯环上有三种不同化学环境的氢原子。
②能发生银镜反应。
(6)以苯和乙烯为原料可合成聚苯乙烯,请设计合成路线(无机试剂及溶剂任选)
注:合成路线的书写格式参照如下示例流程图:
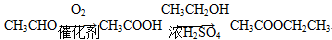
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题9常见金属元素及其重要化合物练习卷(解析版) 题型:填空题
某课外小组对一些金属单质和化合物的性质进行探究。
(1)下表为“铝与氯化铜溶液反应”实验报告的一部分:
实验步骤 | 实验现象 |
将打磨过的铝片(过量)放入一定浓度的CuCl2溶液中 | 产生气泡,析出疏松的红色固体,溶液逐渐变为无色 |
反应结束后分离出溶液备用 | |
红色固体用蒸馏水洗涤后,置于潮湿空气中 | 一段时间后固体由红色变为绿色[设其主要成分为Cu2(OH)2CO3] |
按反应类型写出实验中发生反应的化学方程式各一个(是离子反应的只写离子方程式)
置换反应______________________________________________________;
化合反应______________________________________________________。
(2)用石墨作电极,电解上述实验分离出的溶液,两极产生气泡。持续电解,在阴极附近的溶液中还可以观察到的现象是________________________。
解释此现象的离子方程式是______________________________________。
(3)工业上可用铝与软锰矿(主要成分为MnO2)反应来冶炼金属锰。
①用铝与软锰矿炼锰的原理是(用化学方程式来表示)________________________。
②MnO2在H2O2分解反应中作催化剂。若将适量MnO2加入酸化的H2O2溶液中,MnO2溶解产生Mn2+,该反应的离子方程式是_____________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年高考化学二轮复习 专题6化学反应速率和化学平衡练习卷(解析版) 题型:选择题
在KI溶液中存在下列平衡:I2(aq)+I-(aq) I3— (aq)。测得不同温度下该反应的平衡常数K如表所示:
I3— (aq)。测得不同温度下该反应的平衡常数K如表所示:
t/℃ | 5 | 15 | 25 | 35 | 50 |
K | 1 100 | 841 | 689 | 533 | 409 |
下列说法正确的是 ( )。
A.反应I2(aq)+I-(aq) I3— (aq)的ΔH>0
I3— (aq)的ΔH>0
B.其他条件不变,升高温度,溶液中c(I3—)减小
C.该反应的平衡常数表达式为K=
D.25 ℃时,向溶液中加入少量KI固体,平衡常数K小于689
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com