
【题目】在一固定容积的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:C(s) + 2NO(g) ![]() CO2(g) + N2(g),平衡时c (NO)与温度T的关系如下图所示,则下列说法正确的是
CO2(g) + N2(g),平衡时c (NO)与温度T的关系如下图所示,则下列说法正确的是

A. 该反应的△H>0
B. 若该反应在T1、T2时的平衡常数分别为K1、K2,则K1<K2
C. 若状态B、C、D的压强分别为PB、PC 、PD ,则PC=PD>PB
D. 在T2时,若反应体系处于状态D ,则此时v正>v逆
【答案】D
【解析】
图象是“平衡时c(NO)与温度T的关系”曲线,说明曲线上的每个点对应的状态都是平衡状态,根据平衡移动原理分析。
A.根据题意曲线上每个点对应的状态都处于平衡状态,由图象可知随着温度的升高,c(NO)逐渐增大,说明升温平衡向逆反应方向移动,根据平衡移动原理,该反应的逆反应一定是吸热反应,则其正反应为放热反应即该反应的△H<0,A项错误;
B.该反应的平衡常数K=![]() ,由图象可知T1时c(NO)比T2时c(NO)小,说明T1时平衡正反应进行的程度比T2时大,所以平衡常数K1>K2,B项错误;
,由图象可知T1时c(NO)比T2时c(NO)小,说明T1时平衡正反应进行的程度比T2时大,所以平衡常数K1>K2,B项错误;
C. 由反应式C(s)+2NO(g)![]() CO2(g)+ N2(g)可知反应前后气体分子数不变,在相同温度和容积下,容器中气体压强始终保持不变,所以PB=PD;由于C点对应状态的温度比B点对应状态的温度高,在相同气体分子数和相同容积时压强与温度成正比,所以C点气体压强比B点气体压强大,所以PB=PD<PC,C项错误;
CO2(g)+ N2(g)可知反应前后气体分子数不变,在相同温度和容积下,容器中气体压强始终保持不变,所以PB=PD;由于C点对应状态的温度比B点对应状态的温度高,在相同气体分子数和相同容积时压强与温度成正比,所以C点气体压强比B点气体压强大,所以PB=PD<PC,C项错误;
D.B、D两点对应的温度相同,但D点未达到平衡状态,在保持条件不变时D点自动达到平衡状态即B点状态,因D点容器中c(NO)大于B点容器中c(NO),说明D点将从正反应方向建立平衡,所以此时D点![]() >
>![]() ,D项正确;答案选D。
,D项正确;答案选D。


科目:高中化学 来源: 题型:
【题目】我国古代劳动人民在生产生活中积累了丰富的经验,很多生产过程的操作方法与化学实验中的物质分离除杂方法相似。下列加有着重号的文字与对应分离方法正确的是( )
《本草集经注》 | 《通州煮海录》 | 《名医别录》 | 《续遵义府志》 |
凡渍药酒,皆须细切……便可漉出 | 海陆取卤,日晒火煎,煮海熬波,卤水成盐 | 凡煮汤,欲微火,令小沸……箅渣取液 | 经月画出蒸之……终乃得酒可饮 |
|
|
|
|
A.过滤、蒸馏、萃取、蒸发B.过滤、蒸发、萃取、蒸馏
C.蒸发、萃取、蒸馏、过滤D.萃取、蒸发、过滤、蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍。下列判断正确的是
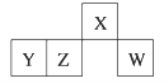
A. 原子半径:rW>rZ>rY>rX B. 含Y元素的盐溶液一定显酸性
C. 最简单气态氢化物的热稳定性:W>X D. Z的最高价氧化物的水化物难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应A2(g) + 2B2(g) ![]() 2AB2(g) △H<0,下列说法正确的是
2AB2(g) △H<0,下列说法正确的是
A. 升高温度,正反应速率增加,逆反应速率减小
B. 增大压强能使正、逆反应速率都增大,但有利于平衡正向移动
C. 达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D. 达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物Y(乙酰氧基胡椒酚乙酸酯)具有抗氧化、抗肿瘤作用,可由化合物X在一定条件下合成:

下列说法正确的是( )
A. X分子中所有原子一定在同一平面上
B. X、Y分子中均含有1个手性碳原子
C. 1molX与溴水充分反应,最多消耗Br2的物质的量为2mol
D. 1molY与NaOH溶液充分反应,最多消耗NaOH的物质的量为4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.5mol·L-1的NaHCO3溶液中滴入酚酞,溶液变红。试回答有关问题:
(1)该溶液中HCO3-的电离程度__________(填“大于”、“小于”或“等于”)HCO3-的水解程度。溶液中Na+、HCO3-、CO32-、H+、OH-离子的浓度由大到小的顺序为______________。
(2)某温度下纯水中的c(H+)= 2×10-7mol/L,则此时溶液中的c(OH-)=_________;若温度不变,滴入稀盐酸,使c(H+)= 5×10-4mol/L,则溶液中c(OH-)=____________,此时溶液中由水电离产生的c(H+)= _________ 。
(3)物质的量浓度均为0.1 mol/L的下列溶液:①KNO3、②Na2CO3、③NaHCO3、④HCl 、⑤CH3COOH、⑥NaOH 、⑦Ba(OH)2、⑧NH4Cl, pH 由大到小的顺序为________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列溶液中,各组离子一定能够大量共存的是
A.使酚酞试液变红的溶液:Na+、Cl-、SO![]() 、Fe3+
、Fe3+
B.使紫色石蕊试液变红的溶液:Fe2+、Mg2+、MnO![]() 、Cl-
、Cl-
C.pH<7的溶液:K+、Ba2+、Cl-、Br-
D.碳酸氢钠溶液:K+、SO![]() 、Cl-、H+
、Cl-、H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列式子属于水解反应,且溶液呈酸性的是 ( )
A. HCO3- + H2O ![]() H3O+ + CO32- B. Fe3+ + 3H2O
H3O+ + CO32- B. Fe3+ + 3H2O ![]() Fe(OH)3 + 3H+
Fe(OH)3 + 3H+
C. HS- + H2O ![]() H2S + OH- D. NH4+ + OH-
H2S + OH- D. NH4+ + OH- ![]() NH3↑+ H2O
NH3↑+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究光盘金属层含有的Ag(其它金属微量忽略不计)、丢弃电池中的Ag2O等废旧资源的回收利用意义重大。下图为从光盘中提取Ag的工业流程。请回答下列问题。

(1)NaClO溶液在受热或酸性条件下易分解,“氧化”阶段需在80℃条件下进行,适宜的加热方式为________。
(2)NaClO溶液与Ag反应的产物为AgCl、NaOH和O2,该反应的化学方程式为________。有人提出以HNO3代替NaClO氧化Ag,从反应产物的角度分析,其缺点是________。
(3)操作Ⅰ的名称为____,简述利用“操作Ⅰ”的装置洗涤难溶物的实验操作________。
(4)化学上常用10%的氨水溶解AgCl固体,AgCl与NH3·H2O按1︰2反应可生成Cl-和一种阳离子________的溶液(填阳离子的化学式)。实际反应中,即使氨水过量也不能将AgCl固体全部溶解,可能的原因是________。
(5)常温时N2H4·H2O(水合肼)在碱性条件下能还原(4)中生成的阳离子,自身转化为无害气体N2,理论上消耗0.1 mol的水合肼可提取到________g的单质Ag。
(6)废旧电池中Ag2O能将有毒气体甲醛(HCHO)氧化成CO2,科学家据此原理将上述过程设计为原电池回收电极材料Ag并有效去除毒气甲醛。则此电池的正极反应式为________,负极的产物有________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com