
取两份铝片,第一份与足量盐酸反应,第二份与足量烧碱溶液反应,同温同压下放出相同体积的气体,则消耗的HCl和NaOH的物质的量之比为( )
A.1∶1 B.2∶1
C.3∶1 D.1∶3
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
(1)0.3 mol NH3分子中所含原子数与________个H2O分子中所含原子数相等。
(2)含有0.4 mol Al3+的Al2(SO4)3溶液中所含SO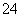 的物质的量是________。
的物质的量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列方程式不能正确解释实验事实的是
A.0.l mol·L-l CH3COOH溶液的pH >1: CH3COOH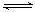 CH3COO-+H+
CH3COO-+H+
B.Na2 CO3溶液能使酚酞试液变红:CO32- +H2O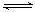 HCO3-+OH-
HCO3-+OH-
C.铁溶于稀硝酸,溶液变黄:3Fe +8H+ +2NO3-=3Fe2++2NO↑+4H2O
D.向Mg(OH)2悬浊液中加入FeCl3溶液,出现红褐色沉淀:
3Mg(OH)2(s)+2Fe3+(aq)=2Fe( OH)3(s)+3Mg2+(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.二氧化硅是酸性氧化物,它可以跟碱反应,但不能与任何酸反应
B.根据反应SiO2+CaCO3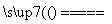 CaSiO3+CO2↑,可推知硅酸的酸性比碳酸的酸性强
CaSiO3+CO2↑,可推知硅酸的酸性比碳酸的酸性强
C.碳酸与硅酸的酸性比较,硅酸酸性弱,且硅酸不溶于水
D.CO2与SiO2均可溶于水生成对应的酸
查看答案和解析>>
科目:高中化学 来源: 题型:
用下列提供的试剂和操作除去各种粉末状混合物中的杂质(括号内为杂质),将序号填在表格内,发生化学反应的写出其反应的化学方程式。
试剂:A.盐酸 B.烧碱溶液 C.氧气 D.水 E.二氧化碳 F.不加其他试剂
操作:(1)加热 (2)加热熔融 (3)高温灼烧 (4)过滤
(5)分液 (6)结晶
| 物质 | 试剂 | 操作 | 有关的化学方程式 |
| ①SiO2(CaCO3) | |||
| ②SiO2(Si) | |||
| ③NaCl(SiO2) | |||
| ④SiO2(NH4Cl) | |||
| ⑤Fe2O3(SiO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查阅有关资料知:金属铝与氢氧化钠溶液反应实际是分以下两步进行:
第一步:2Al+6H2O===2Al(OH)3+3H2↑
第二步:Al(OH)3+NaOH===Na[Al(OH)4]
试回答下列问题:
(1)书写金属铝与氢氧化钠溶液反应的离子方程式:____________________________。
(2)判断两步反应的反应类型:第一步属________,第二步属________(用四种基本反应类型答题)。
(3)请分析,金属铝与氢氧化钠溶液的反应中氧化剂是________,还原剂是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
现代建筑的门窗框架常用电解加工成的古铜色硬铝制造,取硬铝样品进行如下实验(每一步中的试剂均过量):
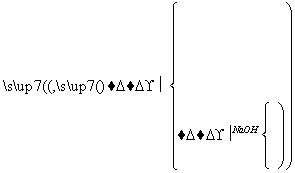
由此可推知,硬铝的组成为( )
A.Al、Cu、Mg、Si、Mn B.Al、Mg、Si、Zn
C.Al、Fe、C、Si D.Al、Si、Zn、Na
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com