
 与
与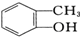
 与
与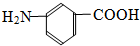
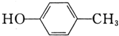 与
与
分析 质子数相同质量数(或中子数)不同的原子互称同位素;
同系物指结构相似、通式相同,组成上相差1个或者若干个CH2原子团,具有相同官能团的化合物;
同种元素形成的不同单质互为同素异形体;
具有相同分子式而结构不同的化合物互为同分异构体;
同一类物质含有的官能团相同.
解答 解:①A、CH2=CH-COOH和油酸(C17H33COOH)结构相似、通式相同,相差1个CH2原子团,互为同系物;
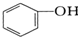
D、 与
与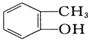 都属于酚类,相差1个CH2原子团,互为同系物;
都属于酚类,相差1个CH2原子团,互为同系物;
故答案为:AD;
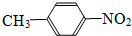
②E. 和
和 F.
F. 和
和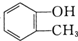 分子式相同,结构不同,属于同分异构体,故答案为:EF;
分子式相同,结构不同,属于同分异构体,故答案为:EF;
③B.乙醇和乙二醇都含有羟基,但羟基的数目不同,不属于同系物,分子式不同,不属于同分异构体;
C.淀粉和纤维素结构不相似,不属于同系物,n值不同,分子式不同,不属于同分异构体;
故答案为:BC.
点评 本题考查“五同”比较以及物质的性质,难度不大,侧重考查学生的辨别能力,选项多,要细心排查,是对心理素质的考验.


科目:高中化学 来源: 题型:解答题
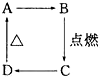 如图中A、B、C、D分别代表有关反应中的一种化合物,其中物质A是一种高熔点化合物,不溶于硫酸、硝酸,却溶于氢氟酸.C为无色无味的气体,能使石灰水变浑浊,D为一种酸,请填写以下空白.
如图中A、B、C、D分别代表有关反应中的一种化合物,其中物质A是一种高熔点化合物,不溶于硫酸、硝酸,却溶于氢氟酸.C为无色无味的气体,能使石灰水变浑浊,D为一种酸,请填写以下空白.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2分子中含有极性键和非极性键 | |
| B. | 向其溶液加入少量MnO2和FeCl3等能加快反应 | |
| C. | H2O2分子中所有原子都达8电子结构 | |
| D. | 该反应中H2O2是氧化剂也是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO3-、OH-、Na+ | B. | Fe2+、OH-、NO3- | C. | Fe2+、H+、Cl- | D. | Fe2+、H+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ① | ⑦ | ④ | ||||
| 3 | ③ | ⑤ | ⑧ | ⑩ | ||||
| 4 | ② | ⑨ |
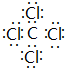 .
.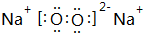 ;④⑧⑨元素的离子的还原性由强到弱顺序为Br->Cl->F-(用离子符号).
;④⑧⑨元素的离子的还原性由强到弱顺序为Br->Cl->F-(用离子符号).查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4 | B. | 3 | C. | 3.5 | D. | 2.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
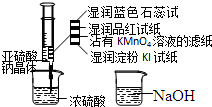 如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )
如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准).则下列有关说法正确的是( )| A. | 湿润淀粉碘化钾试纸未变蓝说明硫元素的非金属性强于碘元素 | |
| B. | 沾有KMnO4溶液的滤纸褪色证明了SO2具有漂白性 | |
| C. | 实验后,可把注射器中的物质缓缓推入NaOH溶液中,以减少环境污染 | |
| D. | 蓝色石蕊试纸变红说明SO2溶于水显酸性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com