
| A. | 0.1mol•L -1AgNO3,溶液:H+、K+、SO42-、I- | |
| B. | c( H+ )/c( OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl- | |
| C. | 由水电离的 c(H+)=1×10-14mol•L-1的溶液中:Ca2+、K+、Cl-、HCO3- | |
| D. | 甲基橙呈红色的溶液中:Na+、CO32-、Fe3+、Cl- |
分析 A.与银离子或硝酸根离子反应的离子不能大量共存;
B.c( H+ )/c( OH-)=1012的溶液呈酸性;
C.由水电离的 c(H+)=1×10-14mol•L-1的溶液可能呈酸性,也可能呈碱性;
D.甲基橙呈红色的溶液呈酸性.
解答 解:A.I-与银离子反应生成沉淀,I-与硝酸根离子在酸性条件下发生氧化还原反应,不能大量共存,故A错误;
B.c( H+ )/c( OH-)=1012的溶液呈酸性,酸性条件下离子之间不发生任何反应,可大量共存,故B正确;
C.由水电离的 c(H+)=1×10-14mol•L-1的溶液可能呈酸性,也可能呈碱性,无论呈酸性还是碱性,HCO3-都不能大量共存,故C错误;
D.甲基橙呈红色的溶液呈酸性,酸性条件下CO32-不能大量共存,故D错误.
故选B.
点评 本题考查离子共存问题,为高考常见题型和高频考点,侧重于学生的分析能力以及元素化合物知识的综合理解和运用的考查,注意把握题目要求以及常见离子的性质和反应类型的判断,答题时注意题给信息,难度不大.


科目:高中化学 来源: 题型:选择题
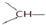 和一个-OH,它的可能结构式有( )
和一个-OH,它的可能结构式有( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
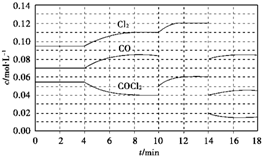
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A2B6 | B. | A2B3 | C. | A3B | D. | AB3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液操作时,先将分液漏斗中的下层液体放出,然后再将上层液体放出 | |
| B. | 用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干 | |
| C. | 用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中 | |
| D. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:
醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下: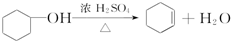
| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.961 8 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.810 2 | 83 | 难溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al(OH)3 | B. | AlCl3 | C. | HCl | D. | NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com