
 .
. 分析 E与FeCl3溶液作用显紫色,证明含有酚羟基,结合分子式知,E是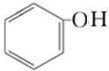 ;E与氢气发生加成反应产生F:
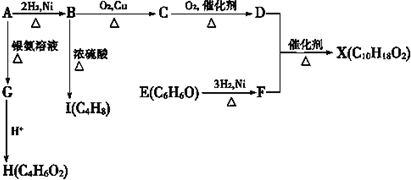
;E与氢气发生加成反应产生F: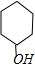 ;A是直连结构,发生一系列反应产生的D与F反应得到X:C10H18O2,X是一种具有水果香味的合成香料,X是酯,则D是CH3CH2CH2COOH;C催化氧化得到丁酸,则C是CH3CH2CH2CHO;B是丁醇CH3CH2CH2CH2OH;由于A能够与银氨溶液发生银镜反应,则A中含有醛基,1mol的A能够与2mol的氢气发生加成反应,则A中还含有一个碳碳双键,则A可能是CH2=CH-CH2CHO或是CH3CH=CHCHO;G则可能是CH2=CH-CH2COONH4或是CH3CH=CHCOONH4;G酸化得到H可能是CH2=CH-CH2COOH或CH3CH=CHCOOH;由于B是丁醇,所以B发生消去反应产生I为CH3CH2CH=CH2,据此分析解答.
;A是直连结构,发生一系列反应产生的D与F反应得到X:C10H18O2,X是一种具有水果香味的合成香料,X是酯,则D是CH3CH2CH2COOH;C催化氧化得到丁酸,则C是CH3CH2CH2CHO;B是丁醇CH3CH2CH2CH2OH;由于A能够与银氨溶液发生银镜反应,则A中含有醛基,1mol的A能够与2mol的氢气发生加成反应,则A中还含有一个碳碳双键,则A可能是CH2=CH-CH2CHO或是CH3CH=CHCHO;G则可能是CH2=CH-CH2COONH4或是CH3CH=CHCOONH4;G酸化得到H可能是CH2=CH-CH2COOH或CH3CH=CHCOOH;由于B是丁醇,所以B发生消去反应产生I为CH3CH2CH=CH2,据此分析解答.
解答 解:E与FeCl3溶液作用显紫色,证明含有酚羟基,结合分子式知,E是 ;E与氢气发生加成反应产生F:
;E与氢气发生加成反应产生F: ;A是直连结构,发生一系列反应产生的D与F反应得到X:C10H18O2,X是一种具有水果香味的合成香料,X是酯,则D是CH3CH2CH2COOH;C催化氧化得到丁酸,则C是CH3CH2CH2CHO;B是丁醇CH3CH2CH2CH2OH;由于A能够与银氨溶液发生银镜反应,则A中含有醛基,1mol的A能够与2mol的氢气发生加成反应,则A中还含有一个碳碳双键,则A可能是CH2=CH-CH2CHO或是CH3CH=CHCHO;G则可能是CH2=CH-CH2COONH4或是CH3CH=CHCOONH4;G酸化得到H可能是CH2=CH-CH2COOH或CH3CH=CHCOOH;由于B是丁醇,所以B发生消去反应产生I为CH3CH2CH=CH2,
;A是直连结构,发生一系列反应产生的D与F反应得到X:C10H18O2,X是一种具有水果香味的合成香料,X是酯,则D是CH3CH2CH2COOH;C催化氧化得到丁酸,则C是CH3CH2CH2CHO;B是丁醇CH3CH2CH2CH2OH;由于A能够与银氨溶液发生银镜反应,则A中含有醛基,1mol的A能够与2mol的氢气发生加成反应,则A中还含有一个碳碳双键,则A可能是CH2=CH-CH2CHO或是CH3CH=CHCHO;G则可能是CH2=CH-CH2COONH4或是CH3CH=CHCOONH4;G酸化得到H可能是CH2=CH-CH2COOH或CH3CH=CHCOOH;由于B是丁醇,所以B发生消去反应产生I为CH3CH2CH=CH2,
(1)C为CH3CH2CH2CHO,其名称是丁醛,B发生消去反应生成I,所以反应类型是消去反应,
故答案为:丁醛;消去反应;
(2)D是丁酸,只含羧基,E是苯酚含有酚羟基;H是丁烯酸,含有碳碳双键和羧基,若只用一种试剂鉴别它们,则该试剂是溴水,与溴水发生反应产生白色沉淀的是苯酚,能够是溴水褪色的是丁烯酸,无任何现象的丁酸,故答案为:溴水;
(3)H丁烯酸与J互为同分异构体,J在酸性条件下水解有乙酸生成,则J是酯,是乙酸乙烯酯,结构简式为CH3COOCH=CH2,
故答案为:CH3COOCH=CH2;
(4)在丁酸分子CH3CH2CH2COOH中含有四种不同的H原子,所以核磁共振氢谱图中D有4组峰且峰面积之比,3:2:2:1,故答案为:4;3:2:2:1;
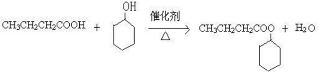
(5)D是丁酸,F是环己醇,二者发生酯化反应,反应方程式为: ,
,
故答案为: .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,根据流程图中物质的分子式、反应条件及某些物质特殊性质进行推断,正确推断各物质结构简式是解本题关键,熟练掌握常见有机物官能团及其性质关系,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 砷的外围电子排布式:3d104S24p3 | |
| B. | 质子数为35、中子数为45的溴原子:${\;}_{35}^{80}$Br | |
| C. | 硫离子的结构示意图: | |
| D. | 过氧化钠的电子式: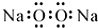 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
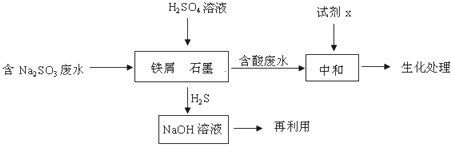
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 粒子代码 | a | I | e |
| 原子核数 | 单核 | 四核 | 双核 |
| 粒子的电荷数 | 一个单位正电荷 | 0 | 一个单位负电荷 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
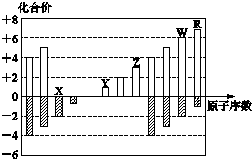
| A. | 离子半径:Z>Y>X | |
| B. | 最高正价氧化物对应的水化物的酸性:R<W | |
| C. | 氢化物的还原性:R>W | |
| D. | R的单质能与W的氢化物反应,可证明非金属性:R>W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将盐卤或石膏加入豆浆中,制成豆腐 | |
| B. | 一支钢笔使用两种不同型号的蓝黑墨水,易出现堵塞 | |
| C. | 三氯化铁溶液中滴稀氨水出现红褐色沉淀 | |
| D. | 清晨,人们经常能看到阳光穿过茂密的树木枝叶所产生的美丽景象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | lmol Cu在适量硫蒸气中燃烧,得到的固体质量为80g | |
| B. | 分子数为NA的CO、C2H4的混合气体体积约为22.4L,质量为28g | |
| C. | 56g Fe投入足量冷的浓硝酸中,转移的电子数为3NA | |
| D. | 0.lmol1${\;}_{53}^{131}$I原子中含电子数为7.8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com