
分析 (1)有颜色的离子不用做实验就能判断是否存在;
(2)加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明含有Ag+;
(3)溶液中一定含银离子,与银离子结合生成沉淀的不能存在.
解答 解:(1)有颜色的离子不用做实验就能判断是否存在,溶液无色说明不含Fe3+,故答案为:Fe3+;
(2)加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失,说明含有Ag+,离子反应方程式为:Ag++Cl-=AgCl↓,故答案为:Ag+;Ag++Cl-=AgCl↓;
(3)原溶液中存在Ag+,则Cl- 不能共存,原溶液中肯定有Mg2+,故CO32-、OH-不能与其共存,硝酸根离子不与所给的任何离子生成沉淀,故溶液中可能大量存在的离子是硝酸根,故选B.
点评 本题主要考查的是离子的检验,为高频考点,侧重于学生的分析、实验和评价能力的考查,根据离子的颜色、离子之间的反应来分析解答,知道铁离子、亚铁离子、硫酸根离子、氯离子、铵根离子的检验方法及现象,题目难度不大.


科目:高中化学 来源: 题型:选择题
 pH=2的A、B两种酸溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示,则列说法不正确的是( )
pH=2的A、B两种酸溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示,则列说法不正确的是( )| A. | A、B两种酸溶液物质的量浓度相等 | B. | 稀释后A酸溶液的酸性比B酸溶液弱 | ||
| C. | 若A=5时,A是强酸,B是弱酸 | D. | 若5>a>2,则A、B都是弱酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2是氧化产物 | |
| B. | H2C2O4在反应中被氧化 | |
| C. | H2C2O4的氧化性强于ClO2的氧化性 | |
| D. | ClO2作水处理剂时,利用了其强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 由于受3d电子的影响,元素周期表中第四周期过渡元素的明显特征是形成多种多样的配合物.
由于受3d电子的影响,元素周期表中第四周期过渡元素的明显特征是形成多种多样的配合物. 分子内的作用力没有B (填编号).
分子内的作用力没有B (填编号).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
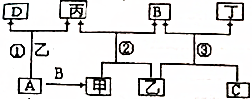 2:1.
2:1.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钙的化学式是Ca2O2 | |
| B. | 1mol过氧化钠和过氧化钙的混合物中,阴影离子数个数比为1:2 | |
| C. | 过氧化钙与足量水反应生成0.5mol氧气时,转移的电子数为2NA | |
| D. | 过氧化钠和过氧化钙都可作漂白剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com