



 ��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1mol������ȫȼ����4mol���� |
| B���붡�黥Ϊͬ���칹�� |
| C����ʹ���Ը��������Һ��ɫ |
| D������ʽΪC3H8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���������Ʒ�Ӧ�ٵķ�Ӧ���õ�һ�ֻ�״���������һ�����ϣ�����������Ľṹ��ʽΪ
���������Ʒ�Ӧ�ٵķ�Ӧ���õ�һ�ֻ�״���������һ�����ϣ�����������Ľṹ��ʽΪ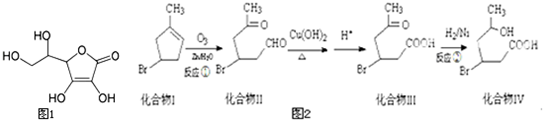
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
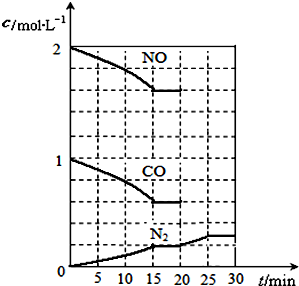 ��������͵������NOx���Դ�����Ⱦ�������أ��о�����������Ⱦ�ķ����ǻ�ѧ�����ߵ���Ҫ���⣬Ŀǰ�кܶ��ַ�������������Ⱦ��
��������͵������NOx���Դ�����Ⱦ�������أ��о�����������Ⱦ�ķ����ǻ�ѧ�����ߵ���Ҫ���⣬Ŀǰ�кܶ��ַ�������������Ⱦ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ͼ�Dz��ֶ�����Ԫ�صĵ��ʼ��仯���������Һ����ת����ϵ����֪B��C��D��E�Ƿǽ������ʣ����ڳ��³�ѹ�¶������壬������G����ɫ��ӦΪ��ɫ��������I��Jͨ��״���³���̬����Ӧ���ǻ��������е�һ����Ҫ�̵���Ӧ��
��ͼ�Dz��ֶ�����Ԫ�صĵ��ʼ��仯���������Һ����ת����ϵ����֪B��C��D��E�Ƿǽ������ʣ����ڳ��³�ѹ�¶������壬������G����ɫ��ӦΪ��ɫ��������I��Jͨ��״���³���̬����Ӧ���ǻ��������е�һ����Ҫ�̵���Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ð�ˮ��ϴ����������Ӧ���Թ� |
| B������е�ʯ��Բ����ƿ�У����뱥��ʳ��ˮ�ɲ�����Ȳ���� |
| C����2%��NaOH��Һ4��5�Σ�����2mL 10%��CuSO4��Һ���Ƶ�Cu��OH��2����Һ��������ȩ��Һ���ȣ����Լ���ȩ������ |
| D����֪��25��ʱ��Ksp[Mg��OH��2]=5.61��10-12��Ksp[MgF2]=7.42��10-11����Mg��OH��2������Һ�м���NaF��Һ��Mg��OH��2������ת����ΪMgF2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���۵�� | B������ |
| C���ܶ�С | D����ѧ���ʻ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com