
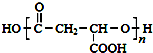 ,合成M的流程图如下:
,合成M的流程图如下: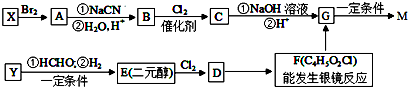
 ,
, .
.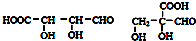 .
. 分析 F发生反应生成G,则G是小分子化合物,G发生缩聚反应生成M,G结构简式为HOOCCH2CH(OH)COOH,C发生取代反应然后酸化得到G,C中含有氯原子,则C结构简式为HOOCCH2CHClCOOH,根据流程图中反应试剂及反应条件知,B为HOOCCH2CH2COOH,A为
X、Y是烃,在核磁共振氢谱图上都只有一个峰,说明都只有一种氢原子,
Y能发生信息②的反应,则Y结构简式为HC≡CH;
根据G结构简式结合F性质知,F结构简式为OHCCH2CHClCHO,E发生取代反应生成D,D中含有氯原子,
则D发生氧化反应生成F,D结构简式为HOCH2CH2CHClCH2OH,E为HOCH2CH2CH2CH2OH,据此分析解答.
解答 解:F发生反应生成G,则G是小分子化合物,G发生缩聚反应生成M,G结构简式为HOOCCH2CH(OH)COOH,C发生取代反应然后酸化得到G,C中含有氯原子,则C结构简式为HOOCCH2CHClCOOH,根据流程图中反应试剂及反应条件知,B为HOOCCH2CH2COOH,A为
X、Y是烃,在核磁共振氢谱图上都只有一个峰,说明都只有一种氢原子,
Y能发生信息②的反应,则Y结构简式为HC≡CH;
根据G结构简式结合F性质知,F结构简式为OHCCH2CHClCHO,E发生取代反应生成D,D中含有氯原子,
则D发生氧化反应生成F,D结构简式为HOCH2CH2CHClCH2OH,E为HOCH2CH2CH2CH2OH,
(1)在X的同系物中,所有碳原子共平面的同系物有丙烯、2-甲基丙烯、2-丁烯、2-甲基-2-丁烯、2、3-二甲基-2-丁烯,所以一共有五种,故答案为:5;
(2)实验室用碳化钙和水反应制取乙炔,反应方程式为CaC2+H2O→Ca(OH)2+C2H2↑,由F生成G可能发生的反应类型有氧化反应、取代反应,
故答案为:CaC2+H2O→Ca(OH)2+C2H2↑;氧化反应、取代反应;
(3)D结构简式为HOCH2CH2CHClCH2OH,其官能团名称是氯原子、羟基,故答案为:氯原子、羟基;
(4)①由G制备M的化学方程式为
②F和足量的新制氢氧化铜悬浊液反应 ,
,
故答案为: ;
; ;
;
(5)G结构简式为HOOCCH2CH(OH)COOH,T是G的同分异构体,T含有三种含氧官能团:羧基、羟基和醛基,两个羟基不连在同一个碳原子上,T可能的结构简式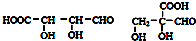 ,
,
故答案为: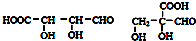 .
.
点评 本题考查有机物推断,侧重考查学生分析推断及知识迁移能力,根据分子式、反应条件及结构简式采用正逆结合的方法进行推断,正确判断物质结构简式是解本题关键,难点是(5)题限制性条件同分异构体结构简式的书写.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
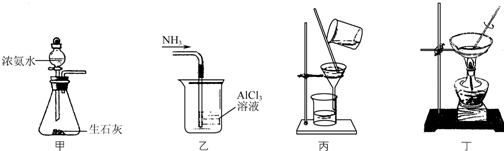
| A. | 用装置甲制取NH3 | |
| B. | 用装置乙吸收NH3制取Al(OH)3 | |
| C. | 用装置丙在不断搅拌下分离Al(OH)3和NH4Cl溶液 | |
| D. | 用装置丁蒸干NH4Cl溶液并灼烧制NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只能被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份,向其中一份中逐渐加入铜粉,最多能溶解19.2g(已知硝酸只能被还原为NO气体).向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示.下列分析或结果错误的是( )| A. | 原混合液中NO3-的物质的量为0.4 mol | |
| B. | OA段产生是NO,AB段反应为2Fe3++Fe=3Fe2+,BC段产生氢气 | |
| C. | 溶液中最终溶质为FeSO4 | |
| D. | c(H2SO4)为5 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ( 2b+2c-a)kJ•mol-1 | B. | (a-2b-2c) kJ•mol-1 | ||
| C. | (b+c-a) kJ•mol-1 | D. | (a-2b-c) kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在$\frac{c({H}^{+})}{c(O{H}^{-})}$=1012的溶液中:Fe2+、Mg2+、NO3-、Cl- | |
| B. | 使甲基橙变红的溶液中:NH4+、Al3+、NO3-、Cl- | |
| C. | 澄清透明的溶液中:ClO-、MnO4-、Al3+、CH3CH2OH | |
| D. | 0.1mol/L的氯化铁溶液中:Na+、SO42-、Cl-、C6H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用pH计、电导率仪(一种测量溶液导电能力的仪器)均可监测乙酸乙酯的水解程度 | |
| B. | 金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理 | |
| C. | 邻苯二甲酸氢钾可用于标定NaOH溶液的浓度,假如称量邻苯二甲酸氢钾时电子天平读数比实际质量偏大,则测得的NaOH溶液浓度比实际浓度偏小 | |
| D. | 高锰酸钾是一种常用的化学试剂,当高锰酸钾晶体结块时,应在研钵中用力研磨,以得到细小晶体,有利于加快反应或溶解的速率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com