
已知电离平衡常数:H2CO3>HClO>HCO3-,氧化性:HClO>Cl2>Br2>Fe3+>I2。下列有关离子反应或离子方程式的叙述中,正确的是( )
| A.能使PH试纸显深红色的溶液中,Fe3+、Cl-、Ba2+、Br-能大量共存 |
| B.向溴水中加入足量氯化亚铁溶液能使溴水变成无色 |
| C.向NaClO溶液中通入少量二氧化碳的离子方程式: 2ClO-+CO2+H2O=2HClO+CO32- |
| D.向FeI2溶液中滴加少量氯水,反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl- |
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省杭州市高三上学期期中七校联考化学试卷 题型:选择题
下列化学用语表示正确的是
A.NaH与重水反应的方程式:NaH+D2O=NaOH +D2↑
B.三氟化氮的电子式: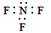
C.含1 mol Ba(OH)2的稀溶液和含1 mol H2SO4的稀溶液反应释放热量akJ,则表示该反应中和热的热化学反应方程式为:OH-(aq)+H+(aq)=H2O(l) H=-a kJ·mol-1
D.次氯酸钠溶液中通入少量的二氧化碳的离子反应方程式:
ClO_ + CO2+ H2O= HClO + HCO3_ 已知电离平衡常数:K(H2CO3)>K(HClO)>K(HCO3-)
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语表示正确的是
A.NaH与重水反应的方程式:NaH+D2O=NaOH+D2↑
B.三氟化氮的电子式:
C.含1 mol Ba(OH)2的稀溶液和含1 mol H2SO4的稀溶液反应释放热量akJ,则表示该反应中和热的热化学反应方程式为:OH-(aq)+H+(aq)=H2O(l) H=-a kJ·mol-1
D.次氯酸钠溶液中通入少量的二氧化碳的离子反应方程式:
ClO_ + CO2+ H2O=HClO + HCO3_ 已知电离平衡常数:K(H2CO3)>K(HClO)>K(HCO3-)
查看答案和解析>>
科目:高中化学 来源:2012届浙江省杭州市高三上学期期中七校联考化学试卷 题型:单选题
下列化学用语表示正确的是
A.NaH与重水 反应的方程式:NaH+D2O="NaOH" +D2↑ 反应的方程式:NaH+D2O="NaOH" +D2↑ |
B.三氟化氮的电子式: |
| C.含1 mol Ba(OH)2的稀溶液和含1 mol H2SO4的稀溶液反应释放热量akJ,则表示该反应中和热的热化学反应方程式为:OH-(aq)+H+(aq)=H2O(l) ?H=-a kJ·mol-1 |
| D.次氯酸钠溶液中通入少量的二氧化碳的离子反应方程式: |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com