
【题目】(12分)中和热的测定是高中重要的定量实验。取0.55 mol/L的NaOH溶液50 mL与0.50 mol/L的盐酸50 mL置于图所示的装置中进行中和热的测定实验,回答下列问题
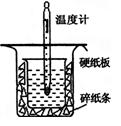
(1)从上图实验装置看,其中尚缺少的一种玻璃用品是_________ _,除此之外,装置中的一个明显错误是 。
(2)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热数值会_________,(填“偏大”、“偏小”或“不变”)。
(3)实验中改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1 NaOH溶液进行反应,与上述实验相比,所求中和热 (填“相等”或“不相等”),简述理由: 。
(4)某实验小组用盐酸和氢氧化钠溶液做了三次实验,每次取溶液各50 mL,并记录下原始数据:
实验序号 | 起始温度t1/℃ | 终止温度(t2)/℃ | 温差(t2-t1)/℃ | ||
盐酸 | NaOH溶液 | 平均值 | |||
1 | 25.1 | 24.9 | 25.0 | 28.3 | 3.3 |
2 | 25.1 | 25.1 | 25.1 | 28.6 | 3.5 |
3 | 25.1 | 25.1 | 25.1 | 27.1 | 2.0 |
已知盐酸、NaOH溶液密度近似为1.00 g/cm3,中和后混合液的比热容c=4.18×10-3 kJ/(g·℃),根据计算结果,写出该中和反应的热化学方程式 。
【答案】
(1)环形玻璃搅拌棒;小烧杯口未用硬纸板盖住(或大烧杯内碎纸条塞少了,未将小烧杯垫的足够高)
(2)偏小
(3)相等 因为计算中和热要折算成生成1 mol H2O所放出的热量(与所用酸、碱的用量无关)
(4)HCl(aq)+NaOH(aq)=NaCl(aq)+H2O(l);△H=-56.85 KJ/mol.
【解析】
试题分析:测定中和热应尽量减少热量的损失,且使酸与碱快速充分反应,(1)从装置图可以看出缺少环形玻璃搅拌棒;小烧杯口未用硬纸板盖住(或大烧杯内碎纸条塞少了,未将小烧杯垫的足够高)会造成热量的损失。(2)醋酸是弱酸,电离过程会吸收热量,则测得的中和热数值会偏小;(3)中和热是指中和生成1 mol H2O所放出的热量(与所用酸、碱的用量无关);(4)分析三组数据,舍去第3组数据,取前两组数据的平均值进行计算,反应生成水的物质的量为0.050L×0.5m ol/L=0.025mol,放出的热量为Q=3.4℃×100g×4.18×10-3 kJ/(g·℃)=1.4212KJ,则中和热△H=-![]() =-56.85 KJ/mol.
=-56.85 KJ/mol.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 正丁烷和异丁烷均有两种一氯取代物
B. 乙烯和苯都能与H2发生加成反应,说明二者的分子中均含碳碳双键
C. 乙醇与金属钠能反应,且在相同条件下比水与金属钠的反应更剧烈
D. 乙醛能被还原成乙醇,但不能被氧化成乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:C(s)+ 1/2O2(g)CO(g) ΔH1 =—110.5 kJ/mol
CO(g)+ 1/2O2(g)CO2(g) ΔH2 = —283.0 kJ/mol
则反应C(s)+O2(g)CO2(g)的反应热为
A. 172.5 kJ/mol B. —172.5 kJ/mol C. 393.5 kJ/mol D. —393.5 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于现行的元素周期表的说法正确的是( )
A.元素周期表有8个副族
B.元素周期表有18个纵行
C.短周期是指第一、二周期
D.ⅠA族的元素全部是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是

A. 图I装置中通入N2和O2的作用是相同的
B. 图Ⅱ中甲、乙两装置产生喷泉的原理一样
C. 图Ⅲ①装置中镁片是原电池的负极;②装置中镁片是原电池的正极
D. 图Ⅳ分液漏斗盛硝酸能证明非金属性N>C>Si,盛硫酸能证明非金属性S>C>Si
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如图:

则M、N相比,较稳定的是 。(用字母“M”或“N”表示)
(2)已知CH3OH(l)的燃烧热△H=-238.6kJ/mol,CH3OH(l)+![]() O2(g)=CO2(g)+2H2(g)△H=-akJ/mol,则a ________238.6(填“>”、“<”或“=”)。
O2(g)=CO2(g)+2H2(g)△H=-akJ/mol,则a ________238.6(填“>”、“<”或“=”)。
(3)使Cl2和H2O(g)通过灼热的炭层生成HCl和CO2,该反应的热化学方程式为____________
2Cl2(g)+2H2O(g)+C(s)=4HCl(g)+CO2(g)△H=-290kJmol﹣1,当有710gCl2参加反应时放出的热量为____________。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,已知4Al(s)+3TiO2(s)+3C(s) =2Al2O3(s)+3TiC(s) △H=-1176kJ/mol,则反应过程中,每转移5mol电子放出的热量为 kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水煤气(CO 和H2)是合成甲醇的重要原料,它可用水蒸气通过炽热的炭层制得:C(s)+H2O(g)![]() CO(g)+H2(g) △H=+131.3kJ/mol
CO(g)+H2(g) △H=+131.3kJ/mol
⑴该反应的平衡常数的表达式为:_________________;升高温度,K值将 ;容器中气体的平均相对分子质量将 。(填“增大”、“减小”或“不变”)。
⑵上述反应达到平衡后,将体系中的C(s)部分移走,平衡将 (填序号)。
A.向左移 B.向右移 C.不移动
⑶下列事实能说明该反应在一定条件下已达到平衡状态的有 (填序号)。
A.单位体积内每消耗1molCO的同时生成1molH2
B.混合气体总物质的量保持不变
C.生成H2O(g)的速率与消耗CO的速率相等
D.H2O(g)、CO、H2的浓度相等
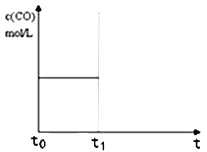
⑷上述反应在t0时刻达到平衡(如图),若在t1时刻改变某一条件,请在图中继续画出t1时刻后c(CO)随时间的变化曲线:
①缩小容器体积(用实线表示)。
②降低温度(用虚线表示)。
⑸某温度下,将4.0mol H2O(g)和足量的炭充入2L的密闭容器中,发生如下反应,C(s)+H2O(g)![]() CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为 。
CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是 ( )
A.已知2SO2(g)+O2![]() 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B.已知C(石墨,s)=C(金刚石,s) △H﹥0,则金刚石比石墨稳定
C.已知H+(aq)+OH–(aq)=H2O(1) △H = -57.3kJ·mol-1,则任何酸碱中和的反应热均为57.3 kJ
D.已知2C(s)+2O2(g)=2CO2(g) △H1,2C(s)+O2(g)=2CO(g) △H2;则△H1﹤△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X的单质是一种理想能源,X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。请回答下列问题:
(1)Y在元素周期表中的位置为__________。
(2)上述元素中,非金属气态氢化物还原性最强的是_________(写化学式);Y和Z形成的含有共价键的化合物的电子式为_________。
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有_________。(写出其中两种物质的化学式)
(4)ZX与水剧烈反应产生X的单质,其化学方程式为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com