
·ÖĪö £Ø1£©BŌ×ÓŗĖĶāµē×ÓŹżĪŖ5£¬øł¾ŻÄÜĮæ×īµĶŌĄķŹéŠ“ŗĖĶāµē×ÓÅŲ¼£»BŹōÓŚµŚ¢óA×åŌŖĖŲ£¬»ÆŗĻ¼ŪĪŖ+3¼Ū£»
£Ø2£©¼ĘĖćBŌ×Ó¼Ū²ćµē×Ó¶ŌŹż”¢¹Āµē×Ó¶ŌŹż£¬Č·¶ØBF3·Ö×Ó”¢BF4-µÄæÕ¼ä½į¹¹£¬ÅŠ¶ĻBF3ÖŠ¼ü½Ē”¢BŌ×ÓŌӻƷ½Ź½£»
£Ø3£©B”¢N¾łŹōÓŚ·Ē½šŹōŌŖĖŲ£¬¶žÕߊĪ³ÉµÄ»Æѧ¼üŹĒ¼«ŠŌ¹²¼Ū¼ü£»øł¾ŻĘä½į¹¹ÓėŹÆÄ«ĻąĖĘ£¬²ćÓė²ćÖ®¼äÓ¦øĆææ·Ö×Ó¼ä×÷ÓĆĮ¦½įŗĻ£»
£Ø4£©Į¢·½µŖ»ÆÅšÖŠµŖŌ×ÓÓėÅšŌ×Ó½»“ķÅÅĮŠ£¬Ę侧Ģå½į¹¹Óė½šøÕŹÆĻąĖĘ£¬Ó²¶ČÓė½šøÕŹÆĻąµ±£¬Į¢·½µŖ»ÆÅšŹōÓŚŌ×Ó¾§Ģ壻½šøÕŹÆ¾§°ūŹĒĮ¢·½Ģ壬ĘäÖŠ8øö¶„µćÓŠ8øöĢ¼Ō×Ó£¬6øöĆęø÷ÓŠ6øöĢ¼Ō×Ó£¬Į¢·½ĢåÄŚ²æ»¹ÓŠ4øöĢ¼Ō×Ó£¬ČēĶ¼ĖłŹ¾£ŗ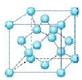 £¬ĖłŅŌ½šøÕŹÆµÄŅ»øö¾§°ūÖŠŗ¬ÓŠµÄĢ¼Ō×ÓŹż=8”Į$\frac{1}{8}$+6”Į$\frac{1}{2}$+4=8£¬Ņņ“ĖĮ¢·½µŖ»ÆÅš¾§°ūÖŠÓ¦øĆŗ¬ÓŠ4øöNŗĶ4øöBŌ×Ó£¬¼ĘĖćBN¾§°ūµÄÖŹĮ攢¾§°ūµÄĢå»ż£¬øł¾Ż¦Ń=$\frac{m}{V}$¼ĘĖćĆÜ¶Č£®
£¬ĖłŅŌ½šøÕŹÆµÄŅ»øö¾§°ūÖŠŗ¬ÓŠµÄĢ¼Ō×ÓŹż=8”Į$\frac{1}{8}$+6”Į$\frac{1}{2}$+4=8£¬Ņņ“ĖĮ¢·½µŖ»ÆÅš¾§°ūÖŠÓ¦øĆŗ¬ÓŠ4øöNŗĶ4øöBŌ×Ó£¬¼ĘĖćBN¾§°ūµÄÖŹĮ攢¾§°ūµÄĢå»ż£¬øł¾Ż¦Ń=$\frac{m}{V}$¼ĘĖćĆÜ¶Č£®
½ā“š ½ā£ŗ£Ø1£©»łĢ¬BŌ×ӵĵē×ÓÅŲ¼Ź½ĪŖ1s22s2sp1£¬BNÖŠBŌŖĖŲµÄ»ÆŗĻ¼ŪĪŖ+3£¬¹Ź“š°øĪŖ£ŗ1s22s2sp1£»+3£»
£Ø2£©BF3ÖŠBŌ×Ó¹Ā¶Ōµē×Ó¶ŌŹż=$\frac{1}{2}$”Į£Ø3-3”Į1£©=0£¬BŌ×ÓŠĪ³É3øö¦Ņ ¼ü£¬ĖłŅŌBF3·Ö×ÓĪŖĘ½ĆęÕżČż½ĒŠĪ£¬¼ü½ĒĪŖ120”ć£¬ŌӻƹģµĄŹżÄæĪŖ3+0=3£¬BŌ×ÓŌӻƷ½Ź½ĪŖsp2£»BF4-ÖŠŠÄŌ×ӵĹĀ¶Ōµē×Ó¶ŌŹż=$\frac{1}{2}$”Į£Ø3+1-4”Į1£©=0£¬BŌ×ÓŠĪ³É4øö¦Ņ ¼ü£¬ĖłŅŌĘä½į¹¹ĪŖÕżĖÄĆęĢ壬¹Ź“š°øĪŖ£ŗ120”ć£»sp2£»ÕżĖÄĆęĢ壻
£Ø3£©B”¢N¾łŹōÓŚ·Ē½šŹōŌŖĖŲ£¬¶žÕߊĪ³ÉµÄ»Æѧ¼üŹĒ¼«ŠŌ¹²¼Ū¼ü£»øł¾ŻŹÆÄ«½į¹¹æÉÖŖĮł·½µŖ»ÆÅš¾§ĢåÖŠ£¬²ćÓė²ćÖ®¼äææ·Ö×Ó¼ä×÷ÓĆĮ¦½įŗĻ£¬¹Ź“š°øĪŖ£ŗ¹²¼Ū¼ü£Ø»ņ¼«ŠŌ¹²¼Ū¼ü£©£»·Ö×Ó¼ä×÷ÓĆĮ¦£»
£Ø4£©Į¢·½µŖ»ÆÅšÖŠµŖŌ×ÓÓėÅšŌ×Ó½»“ķÅÅĮŠ£¬Ę侧Ģå½į¹¹Óė½šøÕŹÆĻąĖĘ£¬Ó²¶ČÓė½šøÕŹÆĻąµ±£¬Į¢·½µŖ»ÆÅšŹōÓŚŌ×Ó¾§Ģ壻½šøÕŹÆ¾§°ūŹĒĮ¢·½Ģ壬ĘäÖŠ8øö¶„µćÓŠ8øöĢ¼Ō×Ó£¬6øöĆęø÷ÓŠ6øöĢ¼Ō×Ó£¬Į¢·½ĢåÄŚ²æ»¹ÓŠ4øöĢ¼Ō×Ó£¬ČēĶ¼ĖłŹ¾£ŗ £¬ĖłŅŌ½šøÕŹÆµÄŅ»øö¾§°ūÖŠŗ¬ÓŠµÄĢ¼Ō×ÓŹż=8”Į$\frac{1}{8}$+6”Į$\frac{1}{2}$+4=8£¬Ņņ“ĖĮ¢·½µŖ»ÆÅš¾§°ūÖŠÓ¦øĆŗ¬ÓŠ4øöNŗĶ4øöBŌ×Ó£¬BN¾§°ūÖŠµÄÖŹĮæĪŖ$\frac{25g}{{N}_{A}}$£¬Ņ»øöĮ¢·½µŖ»ÆÅš¾§°ūµÄĢå»żŹĒ£Ø3.615”Į10-10cm£©3£¬Ņņ“ĖĮ¢·½µŖ»ÆÅšµÄĆܶČ=$\frac{25g}{{N}_{A}}$”Ā£Ø3.615”Į10-10cm£©3=$\frac{25”Į4}{£Ø3.615”Į1{0}^{-10}£©^{3}”Į{N}_{A}}$g•cm-3£¬
£¬ĖłŅŌ½šøÕŹÆµÄŅ»øö¾§°ūÖŠŗ¬ÓŠµÄĢ¼Ō×ÓŹż=8”Į$\frac{1}{8}$+6”Į$\frac{1}{2}$+4=8£¬Ņņ“ĖĮ¢·½µŖ»ÆÅš¾§°ūÖŠÓ¦øĆŗ¬ÓŠ4øöNŗĶ4øöBŌ×Ó£¬BN¾§°ūÖŠµÄÖŹĮæĪŖ$\frac{25g}{{N}_{A}}$£¬Ņ»øöĮ¢·½µŖ»ÆÅš¾§°ūµÄĢå»żŹĒ£Ø3.615”Į10-10cm£©3£¬Ņņ“ĖĮ¢·½µŖ»ÆÅšµÄĆܶČ=$\frac{25g}{{N}_{A}}$”Ā£Ø3.615”Į10-10cm£©3=$\frac{25”Į4}{£Ø3.615”Į1{0}^{-10}£©^{3}”Į{N}_{A}}$g•cm-3£¬
¹Ź“š°øĪŖ£ŗŌ×Ó¾§Ģ壻4£»$\frac{25”Į4}{£Ø3.615”Į1{0}^{-10}£©^{3}”Į{N}_{A}}$£®
µćĘĄ ±¾ĢāŹĒ¶ŌĪļÖŹ½į¹¹µÄ漲飬Éę¼°ŗĖĶāµē×ÓÅŲ¼”¢·Ö×Óæռ乹ŠĶ”¢ŌÓ»ÆĄąŠĶµÄÅŠ¶Ļ”¢¾§°ū½į¹¹ŅŌ¼°¾§°ūµÄÓŠ¹Ų¼ĘĖć£¬£Ø4£©ĪŖŅדķµć£¬×¢ŅāŹģ¼Ē֊ѧ³£¼ū¾§°ū½į¹¹£¬ÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ńõ»ÆĪļ£ŗCuO”¢NO”¢SO2”¢H2O | |
| B£® | ¼ī£ŗNaOH”¢KOH”¢Ba£ØOH£©2”¢Na2CO3 | |
| C£® | ¼īŠŌŃõ»ÆĪļ£ŗNa2O”¢CaO”¢Al2O3”¢Na2O2 | |
| D£® | µē½āÖŹ£ŗKNO3”¢Cl2”¢HCl”¢BaSO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ņ»¶ØĪĀ¶ČŗĶŃ¹ĒæĻĀ£¬ĘųĢ¬ĪļÖŹµÄĢå»żÖ÷ŅŖÓɹ¹³ÉĘųĢåµÄ·Ö×ӵē󊔾ö¶Ø | |
| B£® | “Ó1 L 2 mol/LµÄH2SO4ČÜŅŗÖŠČ”³ö0.5 L£¬øĆČÜŅŗÖŠĒāĄė×ÓµÄÅضČĪŖ4mol/L | |
| C£® | Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬30mLA2ĘųĢåŗĶ10mL B2ĘųĢåĒ”ŗĆĶźČ«·“Ӧɜ³É20mLCĘųĢ壬ŌņC»ÆѧŹ½ĪŖ A3 B»ņB A3 | |
| D£® | Ķ¬ĪĀĶ¬Ń¹ĻĀČĪŗĪĘųĢåµÄ·Ö×Ó¼ä¾ąĄė¼øŗõĻąµČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ĻąĶ¬Ģå»żµÄČĪŗĪĘųĢ嶼ŗ¬ÓŠĻąĶ¬ŹżÄæµÄ·Ö×Ó | |
| B£® | ±ź×¼×“æöĻĀ£¬5L H2SĘųĢåÓė5L NH3µÄŌ×ÓøöŹż±ČĪŖ3£ŗ4£® | |
| C£® | Ķ¬ĪĀĶ¬Ń¹ĻĀĻąĶ¬Ģå»żµÄN2ĘųŗĶCOĘųĢåÓŠĻąĶ¬ĪļÖŹµÄĮ攢ĻąĶ¬µÄÖŹĮæŗĶĻąĶ¬µÄ¶ŌæÕĘųµÄĆÜ¶Č | |
| D£® | ĻąĶ¬ĪĀ¶ČĻĀ£¬ĘųĢåµÄŃ¹Ēæ±ČµČÓŚĘųĢåĢå»żµÄ·“±Č |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CS2ĪŖVŠĪµÄ¼«ŠŌ·Ö×Ó | |
| B£® | ClO3- µÄæռ乹ŠĶĪŖĘ½ĆęČż½ĒŠĪ | |
| C£® | SF6ÖŠSŌ×ÓŗĶ·śŌ×Ó¾łĀś×ć×īĶā²ć8µē×ÓĪČ¶Ø½į¹¹ | |
| D£® | SiF4ŗĶSO32-µÄÖŠŠÄŌ×Ó¾łĪŖsp3Ōӻƣ¬SiF4·Ö×Ó³ŹæÕ¼äÕżĖÄĆęĢ壬SO32-³ŹČż½Ē׶ŠĪ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĒāŃõ»Æ±µČÜŅŗÓėĮņĖį·“Ó¦ Ba2++OH-+H++SO42-=BaSO4”ż+H2O | |
| B£® | ³ĪĒåµÄŹÆ»ŅĖ®ÓėĻ”ŃĪĖį·“Ó¦ Ca£ØOH£©2+2H+=Ca2++2H2O | |
| C£® | Ķʬ²åČėĻõĖįŅųČÜŅŗÖŠ Cu+Ag+=Cu2++Ag | |
| D£® | Ģ¼Ėį±µČÜÓŚĻ”ŃĪĖįÖŠ BaCO3+2H+=Ba2++H2O+CO2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | H2O×÷ÅäĢåŹ±£¬CuÓėH2OŠĪ³É¦Ņ¼ü | B£® | H2OµÄÅäĪ»ÄÜĮ¦“óÓŚNH3 | ||
| C£® | ŅŅ“¼æɼõŠ”Ąė×Ó¾§ĢåµÄČܽā¶Č | D£® | Cu£ØNH3£©4SO4ÓöBaCl2ÓŠ°×É«³ĮµķÉś³É |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Į£×Ó·ūŗÅ | Ļą¶Ō·Ö×Ó£ØŌ×Ó£©ÖŹĮæ | ĆæøöĮ£×ÓµÄÖŹĮæ£Øg/øö£© | 1molĪļÖŹŗ¬ÓŠµÄĮ£×ÓŹż£Øøö£© | 1molĪļÖŹÖŹĮæ£Øg£© |
| C | 1.993”Į10-23 | |||
| Fe | 9.302”Į10-23 | |||
| H2SO4 | 1.628”Į10-22 | |||
| H2O | 2.990”Į10-23 | |||
| Na+ | 3.821”Į10-23 | |||
| OH- | 2.824”Į10-23 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Al3+ H+ HCO3- | B£® | Na+ NO3- Cl- | C£® | H+ OH- SO42- | D£® | Ca2+ K+ CO32- |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com