
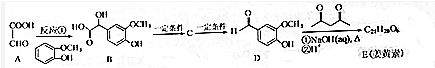
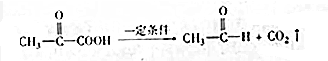


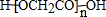
 ��
������ A�����ӳɷ�Ӧ����B��B������Ӧ����C��C��Ӧ����D�����ݵ�һ����Ϣ֪��B������������Ӧ����C��C�ṹ��ʽΪ ��C������Ϣһ�ķ�Ӧ����D��D������Ϣ���ķ�Ӧ����E�ṹ��ʽΪ
��C������Ϣһ�ķ�Ӧ����D��D������Ϣ���ķ�Ӧ����E�ṹ��ʽΪ �������Ŀ�������
�������Ŀ�������
��� �⣺A�����ӳɷ�Ӧ����B��B������Ӧ����C��C��Ӧ����D�����ݵ�һ����Ϣ֪��B������������Ӧ����C��C�ṹ��ʽΪ ��C������Ϣһ�ķ�Ӧ����D��D������Ϣ���ķ�Ӧ����E�ṹ��ʽΪ
��C������Ϣһ�ķ�Ӧ����D��D������Ϣ���ķ�Ӧ����E�ṹ��ʽΪ ��
��
��1��A�к��й������������Ȼ���ȩ������ӦA��B�Ļ�ѧ����ʽ�� ��
��
�ʴ�Ϊ��ȩ�����Ȼ��� ��
��
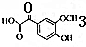
��2��B��C�ķ�Ӧ����Ϊ������Ӧ��C�Ľṹ��ʽΪ ���ʴ�Ϊ��������Ӧ��
���ʴ�Ϊ��������Ӧ�� ��
��
��3��A��������һ�������µļӳɲ���ΪHOCH2COOH��HOCH2COOH�ɷ�Ӧ����һ�ָ߷��ӻ������ṹ��ʽΪ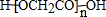 ��
��
�ʴ�Ϊ��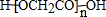 ��
��
��4��E�Ľṹ��ʽΪ ��
��
a��E�к��б������Ѽ������ǻ���̼̼˫�����ʻ�������E�ܷ����������ӳɡ�ȡ���;ۺϷ�Ӧ������ȷ��
b�������Ϸ��ǻ�����λ��ԭ���ܺ��巢��ȡ����Ӧ��̼̼˫���ܺ��巢���ӳɷ�Ӧ������1molE��Ũ��ˮ��Ӧ�������4mol��Br2���ʴ���
c�����з��ǻ�������E����FeCl3��Һ������ɫ��Ӧ������ȷ��
d��ֻ�з��ǻ��ܺ�NaOH��Һ��Ӧ������1molE�������2molNaOH������Ӧ���ʴ���
�ʴ�Ϊ�� ��ac��
��ac��
��5��D��C8H8O3����ͬ���칹���������������
�ٱ����ϵ�һȡ������3�֣�˵�������Ϻ���3����ԭ�ӣ�
��1mol���������������ռ���Һ��Ӧ���������3molNaOH�����з�-OH��ij�ᱽ������
������ȡ�����з�-OH��HCOO-��-CH3��������ǻ��ͼ�λ����λ��������ͬ���칹�壻
������ǻ��ͼ�λ�ڼ�λ��������ͬ���칹�壬������ǻ��ͼ�λ�ڶ�λ��������ͬ���칹�壬
���Է�����������10�֣��ʴ�Ϊ��10��
���� ���⿼���л����ƶϣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������ƶ���������ȷ�����ż������ʹ�ϵ�������Ϣ�ǽⱾ��ؼ����ѵ��ǣ�5����ͬ���칹�������жϣ���Ŀ�Ѷ��еȣ�


 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д� �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�2.24LH2O�з��ӵ���ĿΪ0.1NA | |
| B�� | 0.1mol•L-1NH4Cl��Һ�к���Cl-����ĿΪ0.1NA | |
| C�� | �����£�1.7gNH3�к�����ԭ����ĿΪ0.3 NA | |
| D�� | 5.6g�����������������г��ȼ�գ�ת�Ƶ�����Ϊ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol O2��Na��ȫ��Ӧ��ת�Ƶ�����һ��Ϊ4NA | |
| B�� | 22.4 L NH3�к��й��ۼ�����ĿΪ3NA | |
| C�� | 142 g Na2SO4��Na2HPO4�����������������������3NA | |
| D�� | ��״���£�11.2 L SO3�����ķ�����ĿΪ0.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
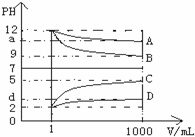
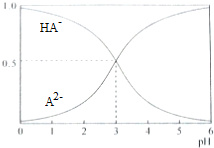 �����£�1mol/L��ij��Ԫ��H2A��Һ�У����ܴ��ڵĺ�A���ӣ�H2A��HA-��A2-�������ʵ���������x����pH�仯�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
�����£�1mol/L��ij��Ԫ��H2A��Һ�У����ܴ��ڵĺ�A���ӣ�H2A��HA-��A2-�������ʵ���������x����pH�仯�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | H2A�ĵ��뷽��ʽΪH2A?H+HA- | |
| B�� | ��pH=2��NaHA��Na2A�����Һ�м�ˮϡ��10������Һ��pH=3 | |
| C�� | ����ͬ���ʵ�����NaHA��Na2A��������ˮ���û����Һ��pHһ��Ϊ3 | |
| D�� | Na2A��Һ���ڣ�c��0H-��=c��H+��+c��HA-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ԭ����ȫ��Ӧ���������CH3CH2Br��NH3�����ʵ���֮��Ϊ2��1 | |
| B�� | CH3CH2Br��HBr�����ڵ���� | |
| C�� | �÷�Ӧ����ȡ����Ӧ | |
| D�� | CH3CH2Br������ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
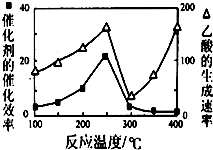 ����CH4��CO2���������ֵ���ߵĻ�ѧ��Ʒ����֪���з�Ӧ��
����CH4��CO2���������ֵ���ߵĻ�ѧ��Ʒ����֪���з�Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com