
| A£®¹²¼Ū»ÆŗĻĪļÖŠø÷Ō×Ó×īĶā²ć¶¼Ņ»¶ØĀś×ć8µē×Ó½į¹¹ |
| B£®BaO2¾§ĢåÖŠŃōĄė×ÓÓėŅõĄė×ÓŹżÄæÖ®±ČĪŖ1”Ć2 |
| C£®H2OŹĒŅ»ÖÖ·Ē³£ĪČ¶ØµÄ»ÆŗĻĪļ£¬ÕāŹĒÓÉÓŚĒā¼üĖłÖĀ |
| D£®ŌŚ·“Ó¦2Na2O2£«2H2O ="=" 4NaOH£«O2”ü£¬¼ČÓŠĄė×Ó¼ü”¢¼«ŠŌ¼üŗĶ·Ē¼«ŠŌ¼üµÄ¶ĻĮŃ£¬ÓÖÓŠĄė×Ó¼ü”¢¼«ŠŌ¼üŗĶ·Ē¼«ŠŌ¼üµÄŠĪ³É |

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ō×Ó°ė¾¶£ŗ±ū>ŅŅ>¼×>¶” |
| B£®¶”»ņ¼×ÓėŅŅĖłŠĪ³ÉµÄ»ÆŗĻĪļ¶¼ŹĒÓŠ¶¾µÄĪļÖŹ |
| C£®×īøß¼ŪŃõ»ÆĪļµÄ¶ŌÓ¦Ė®»ÆĪļµÄĖįŠŌ£ŗ¶”>¼× |
| D£®ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗ¼×>±ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
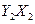 ·Ö×ÓÖŠYŌ×Ó¹ģµĄµÄŌÓ»ÆĄąŠĶĪŖ £¬1mol
·Ö×ÓÖŠYŌ×Ó¹ģµĄµÄŌÓ»ÆĄąŠĶĪŖ £¬1mol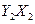 ŗ¬ÓŠ
ŗ¬ÓŠ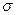 ¼üµÄŹżÄæĪŖ ”£
¼üµÄŹżÄæĪŖ ”£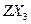 µÄ·Šµć±Č»ÆŗĻĪļ
µÄ·Šµć±Č»ÆŗĻĪļ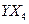 µÄøߣ¬ĘäÖ÷ŅŖŌŅņŹĒ
µÄøߣ¬ĘäÖ÷ŅŖŌŅņŹĒ  ”£
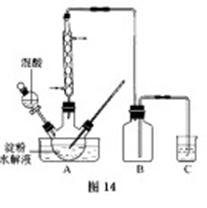
”£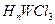 £¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ ”£
£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®13153IŗĶ12753I¶¼ŗ¬ÓŠ55øöÖŠ×Ó |
| B£®13153IŗĶ12753»„ĪŖĶ¬Ī»ĖŲ |
| C£®13153IŗĶ12753IµÄŗĖĶāµē×ÓŹż²»Ķ¬ |
| D£®13153IŗĶ12753I·Ö±šŗ¬ÓŠ131ŗĶ127øöÖŹ×Ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
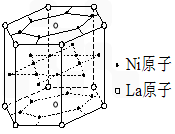
| A£®LaNi6 | B£®LaNi3 | C£®LaNi4 | D£®LaNi5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
| Ö÷×å ÖÜĘŚ | ¢ńA | ¢ņA |  ¢óA ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A | 0×å |
| 2 | | | | ¢Ł | ¢Ś | ¢Ū | | |
| 3 | ¢Ü | | ¢Ż | | | ¢Ž | ¢ß | ¢ą |
| 4 | ¢į | | | | | | | |
 ¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļÖŠ£¬ĖįŠŌ×īĒæµÄ»ÆŗĻĪļµÄ·Ö×ÓŹ½ŹĒ £¬¼īŠŌ×īĒæµÄ»ÆŗĻĪļµÄ»ÆѧŹ½ŹĒ ”£
¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļÖŠ£¬ĖįŠŌ×īĒæµÄ»ÆŗĻĪļµÄ·Ö×ÓŹ½ŹĒ £¬¼īŠŌ×īĒæµÄ»ÆŗĻĪļµÄ»ÆѧŹ½ŹĒ ”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
| µēĄėÄÜ/kJ”¤mol-1 | I1 | I2 | I3 | I4 |
| A | 500 | 4600 | 6900 | 9500 |
| B | 740 | 1500 | 7700 | 10500 |
| C | 580 | 1800 | 2700 | 11600 |
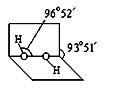
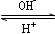 R(OH)3
R(OH)3 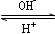 [R(OH)4]£
[R(OH)4]£ C£®·Ē¼«ŠŌ¼ü D£®ÅäĪ»¼ü
C£®·Ē¼«ŠŌ¼ü D£®ÅäĪ»¼ü²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā

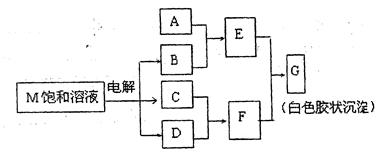
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com