
【化学——选修3:物质结构与性质】(15分)
碳族元素C、Si、Ge的单质及其化合物在材料、医药等方面有重要的应用。请回答下列问题。
(1)Ge原子核外电子排布式为________________________。
(2)C元素的三种单质的晶体结构如图。
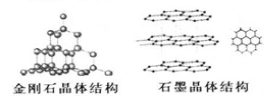
①金刚石晶体中碳原子与碳碳键的个数比为______;石墨晶体中碳原子的杂化类型为__________。
②石墨烯是从石墨材料中剥离出来的、由单层碳原子组成的二维晶体,每个碳原子提供一个p轨道上的电子形成大π键,π电子可以自由移动。将氢气加入到石墨烯中可制得一种新材料石墨烷。下列判断错误的是_______.
A.石墨烯是电的良导体而石墨烷则为绝缘体
B.石墨烯是一种强度很高的材料
C.石墨烯与石墨烷均为高分子化合物
D.石墨烯与H2制得石墨烷的反应属于加成反应
(3)碳元素的电负性比硅元素_______(填“大”或“小”)。CO2分子中碳氧原子之间化学键的成键方式为_________________。
(4)CO可以和很多金属形成配合物,如Ni(CO)4。
①其中Ni与CO之间的键型为_______。Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂,则固态Ni(CO)4属于________晶体。
②与配体CO互为等电子体的阴离子有________(任写一种)。NH3也可作为很多配合物的配体。其中N原子的杂化类型为_____________。若配离子[Ni(NH3)6]2-为正八面体结构,则[Ni(CO)2(NH3)4]2+的结构有____________种。
(1)1s22s22p63s23p63d104s24p2 ;(2)①1:2,sp2;②C;(3)大,σ键和π键 ;(4)①配位键,分子;②CN— 或 C22-,sp3 ,2。
【解析】
试题分析:(1)Ge属于第四周期ⅣA族,原子结构排布式为:1s22s22p63s23p63d104s24p2 ;(2)①金刚石中1个碳原子形成4个共价键,利用均摊法,1个碳原子有2个共价键,碳原子与碳碳键的个数比1:2,石墨中一个碳形成了3个δ键,剩下的1对电子参与了π键的形成,石墨中碳的价层电子对数为3,属于sp2杂化,也可以从石墨中的碳形成平面六元并环结构,sp2杂化形成的是平面结构,即石墨中的碳是sp2杂化;②A、题干中“π电子可以自由移动”,也就是说石墨烯中有自由移动的电子,说明石墨烯能够导电,说法正确;B、石墨烯由单层碳原子组成的二维晶体,使得其具有高强度,说法正确;C、石墨烯有碳原子组成,不是化合物,说法错误;D、石墨烯和氢气反应,破坏π键,使两个氢原子加到两个碳原子上,属于加成反应,说法正确,符合题意的是选项C;(3)根据电负性的规律,同主族从上到下电负性减弱,碳的电负性大于硅的电负性,两个成键原子间只能形成一个δ键,双键中一个δ键一个π键,叁键中一个δ键两个π键,CO2的结构简式:O=C=O,碳氧键有δ键和π键;(4)①Ni提供空轨道,CO提供孤电子对,它们形成的是配位键,常温下为液态说明熔沸点低,又易溶于有机溶剂,体现了分子晶体的特点,固态Ni(CO)4属于分子晶体;②等电子体:原子总数相等、价电子数相同,CO有2个原子、10个价电子,所以与CO互为等电子体的是:N2、CN-、C22-、NO+,等电子体且为阴离子是CN-、C22-,任选一个;NH3中的N有3个δ键,孤对电子=1/2(5-3)=1,价层电子对数为4,所以杂化类型为sp3 , ,有两个CO替代NH3的位置,两个CO邻位,两个CO对位,有2种结构。
,有两个CO替代NH3的位置,两个CO邻位,两个CO对位,有2种结构。
考点:考查核外电子排布式的写法、杂化类型的判断、等电子体、σ键和π键的相关内容。
考点分析: 考点1:物质的结构与性质 试题属性

 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源:2014-2015学年山东省文登市高三第二次统考理科综合化学试卷(解析版) 题型:填空题
(16分)MnO2是重要化学物质,某学习小组设计了将粗MnO2(含有较多的MnO、MnCO3和Fe2O3)样品转化为纯MnO2实验,其流程如下:

按要求回答下列问题
(1) 第②步操作中,氧化性强弱顺序:ClO3-______ MnO2 (填“>”“<”),当NaClO3转移2mol电子时,生成的氧化产物的物质的量为________mol。NaClO3在常温下能够与盐酸反应生成氯气,该反应的离子方程式为___________________。
(2)第④步操作中,最终得到的固体除NaClO3外,还一定含有下列物质中的_________
a.NaCl b.NaClO c.NaClO4 d.NaOH
(3)MnO2是碱性锌锰电池的正极材料,则碱性锌锰电池放电时,正极的电极反应式是:__________。
(4)为得到纯净的MnO2,须将过滤后的MnO2合并后进行洗涤,判断是否洗涤干净可选用的试剂是______(填写一组即可)。工业上可以以石墨为电极电解酸化的硫酸锰制取二氧化锰,该反应的阳极反应式为_____________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省泰安市高三下学期一模理科综合化学试卷(解析版) 题型:填空题
【化学——化学与技术】火山喷发所产生的硫磺可用于生产重要的化工原料——硫酸。某企业用下图所示的工艺流程生产硫酸:
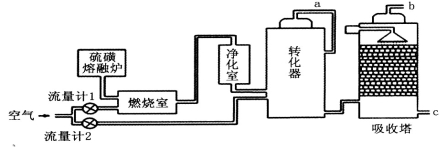
请回答下列问题:
(1)①为充分利用反应放出的热量,转化器中应安装______(填设备名称)。吸收塔中填充有许多瓷管,其作用是________;
②为使硫磺充分燃烧,经流量计l通入燃烧室的氧气过量50%。为提高SO2转化率,经流量计2的氧气量为转化器中二氧化硫完全氧化时理论需氧量的2.5倍,则生产过程中流经流量计l和流量计2的空气体积比应为______。b管排出的尾气的处理方法是________.
③与以硫铁矿为原料的生产工艺相比,该工艺的特点是_________(填字母序号)。
A.耗氧量减少 B.二氧化硫的转化率提高
C.产生的废气减少 D.不需要使用催化剂
(2)硫酸的用途非常广泛;其中可应用于下列哪些方面__________(填字母序号)。
A.橡胶的硫化 B.表面活性剂“烷基苯磺酸钠”的合成
C.铅蓄电池的生产 D.过磷酸钙的制备
(3)矿物燃料的燃烧是产生大气中SO2的主要原因之一。在燃煤中加入适量的石灰石,可有效减少煤燃烧时SO2的排放,请写出此脱硫过程中反应的化学方程式___________________________
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省泰安市高三下学期一模理科综合化学试卷(解析版) 题型:选择题
从下列实验事实所得出的相应结论正确的是
实验事实 | 结论 | |
① | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
② | 将燃烧的镁条放入CO2中能继续燃烧 | 还原性:Mg>C |
③ | NaHCO3溶液与Na[Al(OH)4]溶液混合产生白色沉淀 | 酸性:HCO3->Al(OH)3 |
④ | 常温下白磷可自然而氮气需在放电时才于氧气反应 | 非金属性:P>N |
⑤ | 某无色晶体加入氢氧化钠浓溶液中并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该晶体中一定有NH4+ |
A.②③⑤ B.①②③ C.③④⑤ D.①③⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省稳派教育高三一轮复习质量检测理科综合化学试卷(解析版) 题型:选择题
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X、Y是金属元素,X的焰色呈黄色。五种元素核电荷数之和为49,最外层电子数之和为17;工业上制取金属Y一般通过电解其与W形成的化合物方法;W、Z最外层电子数相同,Z的核电荷数是W的2倍。则下列说法不正确的是
A.Q、W、Z、Y、X原子半径依次增大
B.元素W与元素Z的最高化合价相同
C.Q和X形成的化合物中含有离子键
D.Z元素的简单离子与含有Y元素的离子在水溶液中可能大量共存
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省中山市高三下学期第二次模拟考试理科综合化学试卷(解析版) 题型:实验题
(16分)三草酸合铁酸钾晶体K3[Fe(C2O4)3]3H2O可用于摄影和蓝色印刷。某小组将无水三草酸合铁酸钾在一定条件下加热分解,对所得气体产物和固体产物进行实验和探究。请利用实验室常用仪器、用品和以下限选试剂完成验证和探究过程。
限选试剂:浓硫酸、1.0 mol·L-1 HNO3、1.0 mol·L-1 盐酸、1.0 mol·L-1 NaOH、3% H2O2、0.1 mol·L-1 KI、0.1 mol·L-1 CuSO4、20% KSCN、澄清石灰水、氧化铜、蒸馏水。
(1)该小组同学查阅资料后推知,固体产物中,铁元素不可能以三价形式存在,而盐只有K2CO3。验证固体产物中钾元素存在的方法是 ,现象是 。
(2)固体产物中铁元素存在形式的探究。
①提出合理假设
假设1:全部是铁单质;假设2: ;假设3: 。
②设计实验方案证明你的假设
③实验过程
根据②中方案进行实验。在答题卡上按下表的格式写出实验步骤、预期现象与结论。
实验步骤 | 预期现象与结论 |
步骤1: | 部分固体不溶解 |
步骤2: | |
步骤3:继续步骤2中的(2),进行固液分离,用蒸馏水洗涤固体至洗涤液无色。取少量固体于试管中,滴加过量HCl后,静置,取上层清液,滴加适量H2O2,充分振荡后滴加KSCN。 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省江门市高三3月模拟考试理科综合化学试卷(解析版) 题型:选择题
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
A.0.1mol/LCH3COONa溶液与0.1mol/L HCl溶液等体积混合:c(Na+)>c(Cl-)>c(CH3COO-)>c(OH-)
B.0.1mol/L NH4Cl溶液与0.1mol/L氨水等体积混合(pH>7):c(NH3.H2O)>c(NH4+)>c(Cl-)>c(OH-)
C.0.1mol/L Na2CO3与0.1mol/LNaHCO3溶液等体积混合:2c(Na+)=3c(HCO3-)+3c(CO32-)+3c(H2CO3)
D.0.1mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省长望浏宁四县高三一模考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,下列说法错误的是

A.一定条件下,2molSO2和1molO2混合在密闭容器中充分反应后容器中的分子数大于2NA
B.256g S8分子中含S-S键为7NA个
C.由1molCH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-数目为NA个
D.1 mol Na与O2完全反应,生成Na2O和Na2O2的混合物,转移电子总数为NA个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com