
【题目】某校化学兴趣小组制备消毒液(主要成分是NaClO),设计了下列装置。
已知:Cl2和NaOH溶液能发生下列反应
在加热时:![]()
在低温时:![]()
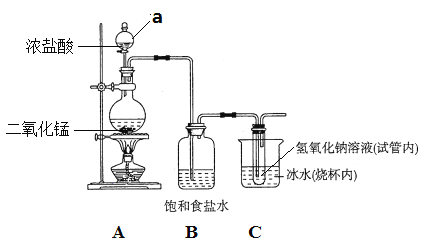
试回答下列问题:
⑴仪器a的名称是_____________。
⑵连接好装置,装药品之前,必须进行的一项操作是_________________。
⑶A装置内发生反应的化学方程式为_______________________________。
⑷B的作用是___________;冰水的作用是__________________________。
⑸该装置的不足之处有___________________________________________。
⑹一定温度下,向NaOH溶液中通入一定量的氯气,二者恰好完全反应。生成物中含有三种含氯元素的离子,其中ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
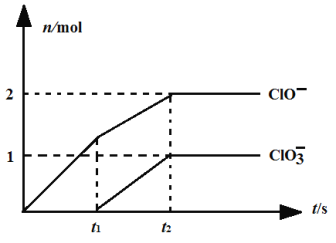
该过程中t2时刻参加反应的Cl2物质的量为_________mol;若另一过程产生的n(Cl-)为5.5mol,n(ClO3-)为1mol,则参加反应的NaOH物质的量为___________________mol。
【答案】分液漏斗 检查实验装置气密性 MnO2 +4HCl(浓)![]() MnCl2 + Cl2↑ +2H2O 除去氯气中的HCl 防止溶液温度升高发生副反应生成NaClO3,降低了产品的产率 没有尾气吸收处理装置 5 7
MnCl2 + Cl2↑ +2H2O 除去氯气中的HCl 防止溶液温度升高发生副反应生成NaClO3,降低了产品的产率 没有尾气吸收处理装置 5 7
【解析】
本题是一道以氯气及其化合物为核心的氧化还原题目,难度一般。
(1)仪器a有塞子和开关,为分液漏斗;
(2)在连接好装置后一定要先检查装置的气密性,若气密性不好则不能继续进行实验;
(3)A装置内发生的就是实验室制氯气的反应,写出方程式即可:![]() ;
;
(4)B中的饱和食盐水可以吸收氯化氢,但是不吸收氯气,因此可以起到除去氯气中的氯化氢的作用;而冰水是为了给![]() 溶液降温,防止溶液温度过高产生氯酸钠等副产物;
溶液降温,防止溶液温度过高产生氯酸钠等副产物;
(5)该装置没有尾气处理装置,而氯气是有毒的,因此需要加一个尾气处理装置;
(6)首先这是一个氯气的歧化反应,因此有![]() 这样一个关系存在,保证反应中得失的电子数一致;而当t2时
这样一个关系存在,保证反应中得失的电子数一致;而当t2时![]() 为2mol,
为2mol,![]() 为1mol,代入关系式解得
为1mol,代入关系式解得![]() 为7mol,因此氯元素一共有10mol,这些氯元素全部是氯气中的,则参加反应的氯气一共有5mol;第二问里代入
为7mol,因此氯元素一共有10mol,这些氯元素全部是氯气中的,则参加反应的氯气一共有5mol;第二问里代入![]() 和
和![]() 的物质的量解出
的物质的量解出![]() 的物质的量为0.5mol,不管是
的物质的量为0.5mol,不管是![]() 、
、![]() 还是
还是![]() ,钠和氯都是1:1的,因此氯一共有7mol,钠也一共有7mol,参加反应的
,钠和氯都是1:1的,因此氯一共有7mol,钠也一共有7mol,参加反应的![]() 也是7mol。
也是7mol。


科目:高中化学 来源: 题型:
【题目】一定量的氢气在氯气中燃烧,所得混合物用100ml 3.0mol/L的NaOH溶液恰好完全吸收,测得溶液中含有NaClO的物质的量为0.05mol。
(1)写出实验室制氯气的化学方程式_______________________________,氧化剂与还原剂的物质的量之比为 ________。
(2)氯气与氢氧化钠溶液反应的离子方程式为 _______________________________ 。
(3)所得溶液中Cl-的物质的量为_____________mol。
(4)原混合物中氯气和氢气的物质的量之比为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中NO产生的反应为:N2(g)+O2(g)![]() 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是:
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是:

A. 温度T下,该反应的平衡常数K=![]()
B. 温度T下,随着反应的进行,混合气体的密度减小
C. 曲线b对应的条件改变可能是加入了催化剂
D. 若曲线b对应的条件改变是温度,可判断该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2催化加氢制甲醇,是极具前景的温室气体资源化研究领域。在某CO催化加氢制甲醇的反应体系中,发生的主要反应有:
i.CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H1=-49.4kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.4kJ·mol-1
ⅱ.CO2(g)+H2(g) ![]() CO(g)+H2O(g) △H2=+41.2kJ·mol-1
CO(g)+H2O(g) △H2=+41.2kJ·mol-1
ⅲ.CO(g)+2H2(g) ![]() CH3OH(g) △H3
CH3OH(g) △H3
(1)△H3________ kJ·mol-1
(2)5MPa时,往某密闭容器中按投料比n(H2):n(CO2)=3:1充入H2和CO2。反应达到平衡时,测得各组分的物质的量分数随温度变化的曲线如图所示。
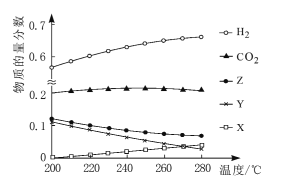
①体系中CO2的物质的量分数受温度的影响不大,原因是____。
②250℃时,反应ii的平衡常数____1(填“>”“<”或“=”)。
③下列措施中,无法提高甲醇产率的是____(填标号)。
A 加入适量CO B 增大压强 C 循环利用原料气 D 升高温度
④如图中X、Y分别代表____(填化学式)。
(3)反应i可能的反应历程如下图所示。
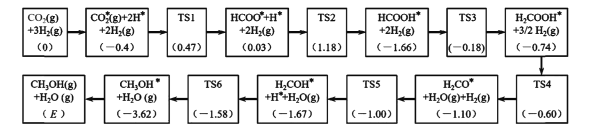
注:方框内包含微粒种类及数目、微粒的相对总能量(括号里的数字或字母,单位:eV)。其中,TS表示过渡态、*表示吸附在催化剂上的微粒。
①反应历程中,生成甲醇的决速步骤的反应方程式为____。
②相对总能量E=____(计算结果保留2位小数)。(已知:leV=1.6×10-22kJ)
(4)用电解法也可实现CO2加氢制甲醇(稀硫酸作电解质溶液)。电解时,往电解池的____极通入氢气,阴极上的电极反应为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】麻黄素M是拟交感神经药。合成M的一种路线如图所示:
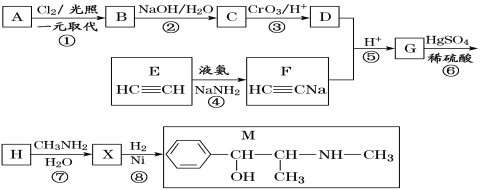
已知:I.R—CH2OH![]() RCHO
RCHO
II.R1-CHO+R-C≡CNa![]()
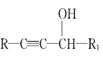
IV.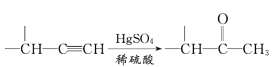
V.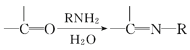
请回答下列问题:
(1)D的名称是_______;G中含氧官能团的名称是_______。
(2)反应②的反应类型为_______;A的结构简式为_______。
(3)写出反应⑦的化学方程式:______________________________。
(4)X分子中最多有_______个碳原子共平面。
(5)在H的同分异构体中,同时能发生水解反应和银镜反应的芳香族化合物中,核磁共振氢谱上有4组峰,且峰面积之比为1∶1∶2∶6的有机物的结构简式为_________________。
(6)已知:![]() 仿照上述流程,设计以苯、乙醛为主要原料合成某药物中间体
仿照上述流程,设计以苯、乙醛为主要原料合成某药物中间体![]() 的路线________________。
的路线________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将11.2g铁粉投入200mL的稀硫酸中,充分反应后,铁粉完全溶解。(假设反应后溶液体积不发生变化,写出计算过程)
⑴求标准状况下产生气体的体积。(已知:Fe+H2SO4=FeSO4+H2↑)_____________
⑵求反应后溶液中FeSO4的物质的量浓度。_________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,反应A(g)+B(g) ![]() C(g)(正反应为放热反应)达到平衡后,根据下列图像判断:
C(g)(正反应为放热反应)达到平衡后,根据下列图像判断:
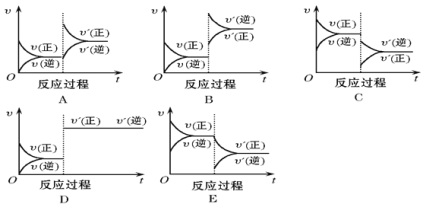
(1)升温,达到新平衡的是________,新平衡中C的体积分数________(填“增大”、“减小”或“不变”,下同)。
(2)降压,达到新平衡的是________,A的转化率________。
(3)减少C的量,达到新平衡的是_______。
(4)增加A的量,达到新平衡的是____,此时B的转化率________,A的转化率________。
(5)使用催化剂,达到平衡的是________, C的质量分数________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《科学美国人》评出的2016年十大创新科技之一的碳呼吸电池,电池原理如下图所示,已知草酸铝[Al2(C2O4)3]难溶于水,则下列说法正确的是

A. 该装置将电能转变为化学能
B. 正极的电极反应为C2O42--2e- =2CO2
C. 每生成 1 mol Al2(C2O4)3,有 6 mol 电子流过负载
D. 随着反应的进行草酸盐浓度不断减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com