
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(CO2)(mol) | 0.4 | 0.35 | 0.31 | 0.3 | 0.3 | 0.3 |
| n(H2)(mol) | 1.2 | 1.05 | n1 | n2 | n2 | n2 |
分析 (1)2s消耗二氧化碳为(0.4-0.31)mol=0.09mol,则消耗氢气为0.09mol×3=0.27mol,进而计算2s时氢气物质的量;
3s时到达平衡,消耗二氧化碳为(0.4-0.3)mol=0.1mol,则:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始量(mol):0.4 1.2 0 0
变化量(mol):0.1 0.3 0.1 0.1
平衡量(mol):0.3 0.9 0.1 0.1
再根据K=$\frac{c(C{H}_{3}OH)×c({H}_{2}O)}{c(C{O}_{2})×{c}^{3}({H}_{2})}$计算平衡常数;
计算1mol二氧化碳反应放出的热量,可以得到反应△H;
(2)转化率=$\frac{物质的量变化量}{起始物质的量}$×100%;
(3)可逆反应到达平衡时,同种物质的正逆速率相等且保持不变,各组分的浓度、含量保持不变,由此衍生的其它一些量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不再变化说明到达平衡;
(4)A.及时分离出产物,反应速率减慢;
B.正反应为放热反应,适当升高温度,平衡逆向移动;
C.增大CO2浓度,反应速率加快,平衡正向移动;
D.选择高效催化剂,不影响平衡移动;
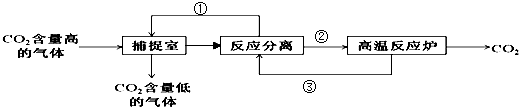
(5)捕捉室中用氢氧化钠吸收二氧化碳得到碳酸钠,将氧化钙加入吸收后溶液中得到碳酸钙与氢氧化钠,通过过滤分离,氢氧化钠循环利用,碳酸钙加热分解得到氧化钙与二氧化碳,CaO再循环利用.
解答 解:(1)2s消耗二氧化碳为(0.4-0.31)mol=0.09mol,则消耗氢气为0.09mol×3=0.27mol,2s时氢气物质的量n1=1.2-0.27=0.93;
3s时到达平衡,消耗二氧化碳为(0.4-0.3)mol=0.1mol,则:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始量(mol):0.4 1.2 0 0
变化量(mol):0.1 0.3 0.1 0.1
平衡量(mol):0.3 0.9 0.1 0.1
容器容积为10L,则平衡常数K=$\frac{c(C{H}_{3}OH)×c({H}_{2}O)}{c(C{O}_{2})×{c}^{3}({H}_{2})}$=$\frac{0.01×0.01}{0.03×0.0{9}^{3}}$=13.7,
1mol二氧化碳反应放出的热量为4.9kJ×$\frac{1mol}{0.1mol}$=49kJ,故反应的△H=-49kJ/mol,
故答案为:0.93;13.7;-49kJ/mol;
(2)二氧化碳转化率=$\frac{0.1mol}{0.4mol}$×100%=25%,
故答案为:25%;
(3)A.v(H2)=3v(CO2),未指明正逆速率,不能说明到达平衡,若分别表示正逆速率,则反应到达平衡,故A错误;
B.随反应进行混合气体物质的量减小,恒温恒容下压强减小,容器内压强保持不变,说明到达平衡,故B正确;
C.v逆(CO2)=v正(CH3OH)说明二氧化碳的消耗速率与生成速率相等,反应到达平衡,故C正确,
D.混合气体总质量不变,容器容积不变,容器内密度始终保持不变,故D错误,
故选:BC;
(4)A.及时分离出产物,平衡正向移动,但反应速率减慢,故A错误;
B.适当升高温度,反应速率加快,正反应为放热反应,平衡逆向移动,故B错误;
C.增大CO2浓度,反应速率加快,平衡正向移动,故C正确;
D.选择高效催化剂,可以加快反应速率,但不影响平衡移动,故D错误,
故选:C;
(5)捕捉室中用氢氧化钠吸收二氧化碳得到碳酸钠,将氧化钙加入吸收后溶液中得到碳酸钙与氢氧化钠,通过过滤分离,氢氧化钠循环利用,碳酸钙加热分解得到氧化钙与二氧化碳,CaO再循环利用,则:
物质①为NaOH,物质③为CaO,操作②为过滤,整个过程发生的化学反应方程式有:
2NaOH+CO2=Na2CO3+H2O,CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
故答案为:NaOH;CaO;过滤;2NaOH+CO2=Na2CO3+H2O,CaO+H2O=Ca(OH)2,Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
点评 本题考查化学平衡计算与影响因素、平衡状态判断、化学工艺流程等,是对学生综合能力的考查,难度中等.


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 实验目的 | 实验方案 |
| A | 验证苯与液溴在溴化铁催化条件下发生的是取代反应 | 将产生的气体物质通入水中,滴入石蕊试液 |
| B | 检验火柴头中氯元素的存在 | 取几根火柴头浸入水中,片刻后再取少量溶液于试管中,滴加硝酸银溶液和稀硝酸 |
| C | 验证Ksp(AgI)<Ksp(AgCl) | 向1L浓度均为0.5mol•L-1NaCl、KI的混合液中滴加AgNO3溶液 |
| D | 配置0.1000mol•L-1CuSO4溶液 | 将12.00g CuSO4•5H20溶于水配成480mL溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
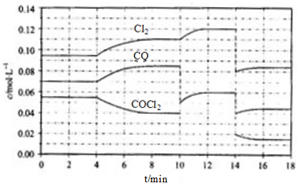 COCl2的分解反应为COCl2(g)?Cl2(g)+CO(g)△H=+108kJ•mol-1.反应体系平衡后,各物质的浓度在不同条件下的变化状况如下图(第10min到14min的COCl2浓度变化曲线未示出):
COCl2的分解反应为COCl2(g)?Cl2(g)+CO(g)△H=+108kJ•mol-1.反应体系平衡后,各物质的浓度在不同条件下的变化状况如下图(第10min到14min的COCl2浓度变化曲线未示出):查看答案和解析>>
科目:高中化学 来源: 题型:解答题
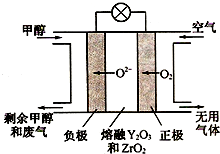 铁元素是重要的金属元素,单质铁在工业和生活中使用得最为广泛.铁还有很多的化合物及其化学反应,如铁与水的反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g)△H
铁元素是重要的金属元素,单质铁在工业和生活中使用得最为广泛.铁还有很多的化合物及其化学反应,如铁与水的反应:3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g)△H| Fe | H2O(g) | Fe3O4 | H2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 1.5 | 1.0 | 1.0 |
| Fe | H2O(g) | Fe3O4 | H2 | |
| 起始/mol | 3.0 | 4.0 | 0 | 0 |
| 平衡/mol | m | n | p | q |
| Fe | H2O(g) | Fe3O4 | H2 | |
| A/mol | 3.0 | 4.0 | 0 | 0 |
| B/mol | 0 | 0 | 1.0 | 4.0 |
| C/mol | m | n | p | q |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
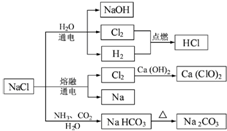
| A. | 25℃,NaHCO3在水中的溶解度比Na2CO3的大 | |
| B. | 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 | |
| C. | 常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 | |
| D. | 图中所示转化反应不都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com