
 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:| 1000ω |
| M |
| n |
| V |
| 1000×1.2g/ml×36.5% |
| 36.5g/mol |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、开始加入合金的物质的量之和为0.3mol |
| B、反应中被还原和未被还原的硝酸物质的量之比为3:1 |
| C、沉淀完全时消耗NaOH溶液的体积为200mL |
| D、生成沉淀的质量比原合金的质量增加10.2g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该物质属于不饱和烃 |
| B、该分子碳、氮原子均满足8电子结构 |
| C、该分子所有原子处在一条直线上 |
| D、1mol该物质在一定条件下可与8molH2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①④⑤ | B、①②④ |
| C、③④⑤ | D、①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KMnO4 |
| B、KClO3 |
| C、CaCl2 |
| D、Ca(ClO)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
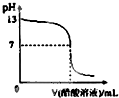 常温下,向10mL 0.1mol?L-1NaOH溶液中逐滴加入0.1mol?L-1醋酸溶液,所得滴定曲线如图所示.下列说法正确的是( )
常温下,向10mL 0.1mol?L-1NaOH溶液中逐滴加入0.1mol?L-1醋酸溶液,所得滴定曲线如图所示.下列说法正确的是( )| A、pH=7时,所加醋酸溶液的体积为10mL |
| B、pH<7时,溶液中c(CH3COO-)<c(Na+) |
| C、醋酸滴入10ml时,c(Na+)═c(CH3COOH)+c(CH3COO-) |
| D、继续滴加0.1 mol?L-1醋酸溶液,溶液pH可以变为1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、漂白精的有效成分是NaClO |
| B、碘化钾的水溶液遇淀粉现蓝色 |
| C、硫在空气中燃烧生成SO2,在纯氧中生成SO3 |
| D、漂白精露置空气中变质,既发生氧化反应又发生非氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com