
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
| n(CO) | n(H2O) | n(H2) | n(CO2) | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |
| 2×3 |
| 1×5 |
| 1×1 |
| 2×2 |
| 0×0 |
| 3×3 |
| 1×1 |
| 0.5×2 |
| 2×1 |
| 3×1 |
| 2 |
| 3 |
| c(CO)?c(H2) |
| c(H2O) |
| c(H2)?c(CO2) |
| c(CO)?c(H2O) |
| c2(CO) |
| c(CO2) |
| K1 |
| K2 |
| K1 |
| K2 |
| (0.01-x)2 |
| (x)2 |
| 0.01-0.0025 |
| 0.01 |
| y(1-x)?y(1-x) |
| (1-x)?(1-y)?[x-y(1-x)] |


科目:高中化学 来源: 题型:
 4.53g硫酸铝铵晶体加热分解,最终剩余0.51g Al2O3固体.加热过程中,固体质量随温度的变化如图所示.请通过计算确定400℃时剩余固体成分的化学式(写出计算过程).
4.53g硫酸铝铵晶体加热分解,最终剩余0.51g Al2O3固体.加热过程中,固体质量随温度的变化如图所示.请通过计算确定400℃时剩余固体成分的化学式(写出计算过程).查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶质增加了3.5g |
| B、氢氧化钠的物质的量不变,而水被电解了1mol |
| C、氢氧化钠的消耗比水的消耗少 |
| D、氢氧化钠不参加反应,只有水参加反应,且放出H2和O2,消耗了18g水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
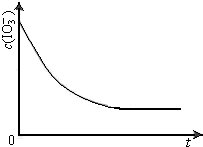 “粤盐”精制盐的食品添加剂为KIO3、K4[Fe(CN)6](亚铁氰化钾);碘在科研与生活中有重要应用.
“粤盐”精制盐的食品添加剂为KIO3、K4[Fe(CN)6](亚铁氰化钾);碘在科研与生活中有重要应用.| 实验 序号 | 体积V/mL | ||||
| KIO3溶液 | 水 | H2SO4溶液 | Na2SO3溶液 | 淀粉溶液 | |
| ① | 12.0 | 0.0 | 6.0 | 10.0 | 2.0 |
| ② | 10.0 | X | 6.0 | 10.0 | 2.0 |
| ③ | 11.0 | 1.0 | 6.0 | 10.0 | 2.0 |
| 序号 | 实验操作 | 实验现象 | 结论 |
| ① | 取少量精制盐样品于洁净试管中,加入适量蒸馏水 | 得到无色溶液 | |
| ② | 试样含有K+ | ||
| ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、45ml | B、30ml |
| C、42.5ml | D、60ml |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.336升 |
| B、0.224升 |
| C、0.896升 |
| D、1.12升 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.3g | B、3.1g |
| C、4.6g | D、5.3g |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com