
”¾ĢāÄæ”æ(1)ŌŚ101 kPaŹ±£¬H2ŌŚ1 mol O2ÖŠĶźČ«Č¼ÉÕÉś³É2 molŅŗĢ¬Ė®£¬·Å³ö571.6 kJµÄČČĮ棬±ķŹ¾H2Č¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½ĪŖ__________________________”£
(2)1.00 L 1.00 mol”¤L£1ĮņĖįÓė2.00L 1.00 mol”¤L£1 NaOHČÜŅŗĶźČ«·“Ó¦£¬·Å³ö114.6 kJµÄČČĮ棬øĆ·“Ó¦µÄÖŠŗĶČČĪŖ±ķŹ¾ĘäÖŠŗĶČȵÄČČ»Æѧ·½³ĢŹ½ĪŖ________________”£
(3)0.3 molĘųĢ¬øßÄÜČ¼ĮĻŅŅÅšĶé(B2H6)ŌŚŃõĘųÖŠČ¼ÉÕ£¬Éś³É¹ĢĢ¬ČżŃõ»Æ¶žÅšŗĶŅŗĢ¬Ė®£¬·Å³ö649. 5 kJČČĮ棬ĘäČČ»Æѧ·½³ĢŹ½ĪŖ________________________£»ÓÖŅŃÖŖH2O(l)===H2O(g)””¦¤H£½£«44 kJ”¤mol£1£¬Ōņ11.2L(±ź×¼×“æö)ŅŅÅšĶéĶźČ«Č¼ÉÕÉś³ÉĘųĢ¬Ė®Ź±·Å³öµÄČČĮæŹĒ________kJ”£
”¾“š°ø”æH2(g)£«1/2O2(g)===H2O(l)””¦¤H£½£285.8 kJ”¤mol£1 1/2 H2SO4(aq)£«NaOH(aq)===1/2Na2SO4(aq)£«H2O(l)””¦¤H£½£57.3 kJ”¤mol£1 B2H6(g)£«3O2(g)===B2O3(s)£«3H2O(l)””¦¤H£½£2 165 kJ”¤mol£1 1 016.5
”¾½āĪö”æ
(1) Č¼ÉÕČČŹĒÖøŌŚ101 kPaŹ±£¬1molæÉČ¼ĪļĶźČ«Č¼ÉÕÉś³ÉĪČ¶ØµÄŃõ»ÆĪļŹ±µÄ·“Ó¦ČČ”£ÓÉŅŃÖŖŌŚ101 kPaŹ±£¬2molH2ŌŚ1 mol O2ÖŠĶźČ«Č¼ÉÕÉś³É2 molŅŗĢ¬Ė®£¬·Å³ö571.6 kJµÄČČĮ棬ĖłŅŌH2Č¼ÉÕČȵÄČČ»Æѧ·½³ĢŹ½ĪŖH2(g)£«1/2O2(g) =H2O(l)””¦¤H£½£285.8 kJ”¤mol£1”£“š°ø£ŗH2(g)£«1/2O2(g)=H2O(l)””¦¤H£½£285.8 kJ”¤mol£1”£
£Ø2£©ÖŠŗĶ·“Ó¦µÄ·“Ó¦ČČŅŌÉś³É1molŅŗĢ¬H2OĪŖ±ź×¼£¬¶ų1.00 L 1.00 mol”¤L£1ĮņĖįÓė2.00L 1.00 mol”¤L£1 NaOHČÜŅŗ·“Ӧɜ³É2molŅŗĢ¬H2O·Å³ö114.6 kJµÄČČĮ攣֊ŗĶČČ»Æѧ·½³ĢŹ½ĪŖ1/2 H2SO4(aq)£«NaOH(aq)=1/2Na2SO4(aq)£«H2O(l)””¦¤H£½£57.3 kJ”¤mol£1“š°ø£ŗ1/2 H2SO4(aq)£«NaOH(aq)=1/2Na2SO4(aq)£«H2O(l)””¦¤H£½£57.3 kJ”¤mol£1 ”£
(3)1molB2H6(g)ĶźČ«Č¼ÉÕ£¬Éś³ÉŅŗĢ¬Ė®·Å³öµÄČČĮæĪŖ649. 5 kJ /0.3 mol=2165kJ £¬Ņņ“ĖČČ»Æѧ·½³ĢŹ½ĪŖB2H6(g)£«3O2(g)=B2O3(s)£«3H2O(l)””¦¤H£½£2 165 kJ”¤mol£1”£Čō·“Ӧɜ³ÉµÄ3molH2O(l)Č«²æ×Ŗ»ÆĪŖĘųĢ¬Ė®£¬ŌņŠčĪüŹÕČČĮæ44 kJ”¤mol£1![]() kJ£¬11.2L(±ź×¼×“æö)ŅŅÅšĶéĪŖ0.5mol,Ōņ0.5mol B2H6(g)ĶźČ«Č¼ÉÕÉś³ÉĘųĢ¬Ė®Ź±·Å³öµÄČČĮæĪŖ(2 165 -
kJ£¬11.2L(±ź×¼×“æö)ŅŅÅšĶéĪŖ0.5mol,Ōņ0.5mol B2H6(g)ĶźČ«Č¼ÉÕÉś³ÉĘųĢ¬Ė®Ź±·Å³öµÄČČĮæĪŖ(2 165 -![]() )
)![]() 0.5/1= 1 016.5kJ”£“š°ø£ŗB2H6(g)£«3O2(g)=B2O3(s)£«3H2O(l)””¦¤H£½£2 165 kJ”¤mol£1 ”¢ 1 016.5”£
0.5/1= 1 016.5kJ”£“š°ø£ŗB2H6(g)£«3O2(g)=B2O3(s)£«3H2O(l)””¦¤H£½£2 165 kJ”¤mol£1 ”¢ 1 016.5”£


 æŚĖćĢāæؼÓÓ¦ÓĆĢā¼ÆѵĻµĮŠ“š°ø
æŚĖćĢāæؼÓÓ¦ÓĆĢā¼ÆѵĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij³§ÅųöµÄ·ĻŅŗÖ÷ŅŖŗ¬ÓŠĻõĖįŠæŗĶĻõĖįŅų£¬ĪŖĮĖ“ÓÖŠ»ŲŹÕ½šŹōŅųŗĶĻõĖįŠæ£¬Ä³ÖŠŃ§»ÆѧæĪĶā»ī¶ÆŠ”×éÉč¼ĘĮĖŅŌĻĀµÄŹµŃé²½Öč£ŗ

(1)XŹĒ____________£¬YŹĒ____________ (Š“»ÆѧŹ½£¬ĻĀĶ¬)”£
(2)¹ĢĢåA”¢ĀĖŅŗB”¢CµÄÖ÷ŅŖ³É·Ö£ŗA______________£¬B______________£¬C______________”£
(3)Z“¦½ųŠŠµÄ²Ł×÷ŹĒ__________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĆŗČ¼ÉÕÅŷŵÄŃĢĘųŗ¬ÓŠSO2ŗĶNOx£¬ŠĪ³ÉĖįÓź”¢ĪŪČ¾“óĘų£¬²ÉÓĆNaClO2ČÜŅŗ×÷ĪŖĪüŹÕ¼ĮæÉĶ¬Ź±¶ŌŃĢĘų½ųŠŠĶŃĮņ”¢ĶŃĻõ£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£© NaClO2µÄ»ÆѧĆū³ĘĪŖ_______”£
£Ø2£©ŌŚ¹ÄÅŻ·“Ó¦Ę÷ÖŠĶØČėŗ¬ÓŠŗ¬ÓŠSO2ŗĶNOxµÄŃĢĘų£¬·“Ó¦ĪĀ¶ČĪŖ323 K£¬NaClO2ČÜŅŗÅضČĪŖ5”Į103mol”¤L1”£·“Ó¦Ņ»¶ĪŹ±¼äŗóČÜŅŗÖŠĄė×ÓÅØ¶ČµÄ·ÖĪö½į¹ūČēĻĀ±ķ”·
Ąė×Ó | SO42 | SO32 | NO3 | NO2 | Cl |
c/£Ømol”¤L1£© | 8.35”Į104 | 6.87”Į106 | 1.5”Į104 | 1.2”Į105 | 3.4”Į103 |
¢ŁŠ“³öNaClO2ČÜŅŗĶŃĻõ¹ż³ĢÖŠÖ÷ŅŖ·“Ó¦µÄĄė×Ó·½³ĢŹ½__________”£Ōö¼ÓŃ¹Ē棬NOµÄ×Ŗ»ÆĀŹ______£ØĢī”°Ģįøß”±”°²»±ä”±»ņ”°½µµĶ”±£©”£
¢ŚĖę×ÅĪüŹÕ·“Ó¦µÄ½ųŠŠ£¬ĪüŹÕ¼ĮČÜŅŗµÄpHÖš½„______ £ØĢī”°Ģįøß”±”°²»±ä”±»ņ”°½µµĶ”±£©”£
¢ŪÓÉŹµŃé½į¹ūæÉÖŖ£¬ĶŃĮņ·“Ó¦ĖŁĀŹ______ĶŃĻõ·“Ó¦ĖŁĀŹ£ØĢī”°“óÓŚ”±»ņ”°Š”ÓŚ”±£©”£ŌŅņŹĒ³żĮĖSO2ŗĶNOŌŚŃĢĘųÖŠµÄ³õŹ¼ÅØ¶Č²»Ķ¬£¬»¹æÉÄÜŹĒ___________”£
£Ø3£©ŌŚ²»Ķ¬ĪĀ¶ČĻĀ£¬NaClO2ČÜŅŗĶŃĮņ”¢ĶŃĻõµÄ·“Ó¦ÖŠ£¬SO2ŗĶNOµÄĘ½ŗā·ÖŃ¹pxČēĶ¼ĖłŹ¾”£
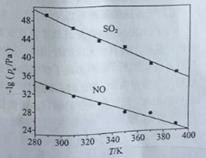
¢ŁÓÉĶ¼·ÖĪöæÉÖŖ£¬·“Ó¦ĪĀ¶ČÉżøߣ¬ĶŃĮņ”¢ĶŃĻõ·“Ó¦µÄĘ½ŗā³£Źż¾ł______________£ØĢī”°Ōö“ó”±”°²»±ä”±»ņ”°¼õŠ””±£©”£
¢Ś·“Ó¦ClO2+2SO32===2SO42+ClµÄĘ½ŗā³£ŹżK±ķ“ļŹ½ĪŖ___________”£
£Ø4£©Čē¹ū²ÉÓĆNaClO”¢Ca£ØClO£©2Ģę“śNaClO2£¬Ņ²ÄܵƵ½½ĻŗƵÄŃĢĘųĶŃĮņŠ§¹ū”£
¢Ł“Ó»ÆŃ§Ę½ŗāŌĄķ·ÖĪö£¬Ca£ØClO£©2Ļą±ČNaClO¾ßÓŠµÄÓŠµćŹĒ_______”£
¢ŚŅŃÖŖĻĀĮŠ·“Ó¦£ŗ
SO2£Øg£©+2OH£Øaq£© ===SO32£Øaq£©+H2O£Øl£© ¦¤H1
ClO£Øaq£©+SO32£Øaq£© ===SO42£Øaq£©+Cl£Øaq£© ¦¤H2
CaSO4£Øs£© ===Ca2+£Øaq£©+SO42£Øaq£© ¦¤H3
Ōņ·“Ó¦SO2£Øg£©+ Ca2+£Øaq£©+ ClO£Øaq£© +2OH£Øaq£© ="==" CaSO4£Øs£© +H2O£Øl£© +Cl£Øaq£©µÄ¦¤H=______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°ŃĶ¼2µÄĖéÖ½Ę¬²¹³äµ½Ķ¼1ÖŠ£¬æɵƵ½Ņ»øöĶźÕūµÄŃõ»Æ»¹Ō·“Ó¦µÄĄė×Ó·½³ĢŹ½£ØĪ“ÅäĘ½£©”£ĻĀĮŠ¶ŌøĆ·“Ó¦µÄĖµ·Ø²»ÕżČ·µÄŹĒ

A. IO4©×÷Ńõ»Æ¼Į
B. ČōÓŠ1 mol Mn2+²Ī¼Ó·“Ó¦×ŖŅĘ5molµē×Ó
C. »¹Ō¼ĮÓėŃõ»Æ¼ĮµÄĪļÖŹµÄĮæÖ®±ČĪŖ2£ŗ5
D. ÅäĘ½ŗóH+”¢Mn2+µÄ»Æѧ¼ĘĮæŹż·Ö±šĪŖ4”¢2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ2 LĆܱÕČŻĘ÷ÖŠ£¬800”ꏱ·“Ó¦2NO(g)£«O2(g) ![]() 2NO2(g)ĢåĻµÖŠ£¬n(NO)Ėꏱ¼äµÄ±ä»ÆČēĻĀ±ķ£ŗ
2NO2(g)ĢåĻµÖŠ£¬n(NO)Ėꏱ¼äµÄ±ä»ÆČēĻĀ±ķ£ŗ
Ź±¼ä/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)Š“³öøĆ·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½£ŗK£½________£¬ŅŃÖŖ£ŗK(300”ę)>K(350”ę)£¬øĆ·“Ó¦ŹĒ________·“Ó¦(Ģī”°·ÅČČ”±»ņ”°ĪüČČ”±)”£
(2)ĻĀĶ¼ÖŠ±ķŹ¾NO2µÄ±ä»ÆµÄĒśĻߏĒ___£¬ÓĆO2µÄÅØ¶Č±ä»Æ±ķŹ¾“Ó0”«2 sÄŚøĆ·“Ó¦µÄĘ½¾łĖŁĀŹv£½__________”£

(3)ÄÜĖµĆ÷øĆ·“Ó¦ŅŃ¾“ļµ½Ę½ŗāדĢ¬µÄŹĒ£Ø____£©
a£®v(NO2)£½2v(O2) b£®ČŻĘ÷ÄŚŃ¹Ēæ±£³Ö²»±ä
c£®vÄę(NO)£½2vÕż(O2) d£®ČŻĘ÷ÄŚĪļÖŹµÄĆܶȱ£³Ö²»±ä
(4)ÄÜŹ¹øĆ·“Ó¦µÄ·“Ó¦ĖŁĀŹŌö“ó£¬ĒŅĘ½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶ÆµÄŹĒ£Ø____£©
a£®¼°Ź±·ÖĄė³öNO2ĘųĢå b£®ŹŹµ±ÉżøßĪĀ¶Č
c£®Ōö“óO2µÄÅØ¶Č d£®Ń”Ōńøߊ§µÄ“߻ƼĮ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄÜŌ“æÉ»®·ÖĪŖŅ»“ĪÄÜŌ“ŗĶ- ¶ž“ĪÄÜŌ“£¬Ö±½Ó“Ó×ŌČ»½ēČ”µĆµÄÄÜŌ“³ĘĪŖŅ»¼¶ÄÜŌ“£¬Ņ»“ĪÄÜŌ“¾¹ż¼Ó¹¤”¢×Ŗ»»µĆµ½µÄÄÜŌ“³ÉĪŖ:¶ž“ĪÄÜŌ“”£ĻĀĮŠÄÜŌ“ÖŠŹōÓŚŅ»“ĪÄÜŌ“µÄŹĒ
A. ĒāÄÜB. µēÄÜC. ŗĖÄÜD. Ė®ĆŗĘų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A. ·ēÄÜ”¢Ģ«ŃōÄܵȏōÓŚŅ»“ĪÄÜŌ“
B. X![]() Y£«ZÕż·“Ó¦ĪüČČ£¬ŌņÄę·“Ó¦±ŲČ»·ÅČČ
Y£«ZÕż·“Ó¦ĪüČČ£¬ŌņÄę·“Ó¦±ŲČ»·ÅČČ
C. »Æѧ·“Ó¦µÄģŹ±ä¦¤HŌ½“󣬱ķŹ¾·ÅČČŌ½¶ą
D. Ļ”ČÜŅŗÖŠ£¬Ėį¼īÖŠŗĶ·“Ӧɜ³É1 mol H2OŹ±·ÅČČ²»Ņ»¶ØĪŖ57.3 kJ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀ±ķĪŖŌŖĖŲÖÜĘŚ±ķµÄŅ»²æ·Ö£¬Ēė»Ų“šÓŠ¹ŲĪŹĢā£ŗ

£Ø1£©¢ŻŗĶ¢ąµÄŌŖĖŲ·ūŗÅŹĒ________ŗĶ________(ĢīŠ“ŌŖĖŲ·ūŗÅ£¬ĻĀĶ¬)£»
£Ø2£©±ķÖŠ×ī»īĘĆµÄ½šŹōŹĒ________£¬·Ē½šŹō×īĒæµÄŌŖĖŲŹĒ________£»
£Ø3£©¢ŽµÄ×īøßÕż¼ŪŹĒ________”£
£Ø4£©¢ßŗĶ¢āµ„ÖŹŃõ»ÆŠŌ________Ēæ(ĢīŠ“ŌŖĖŲ·ūŗÅ)£»
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¾ö¶Ø»Æѧ·“Ó¦ĖŁĀŹµÄÖ÷ŅŖŅņĖŲŹĒ£ŗ
A. “߻ƼĮB. ·“Ó¦ĪļµÄŠŌÖŹ
C. ĪĀ¶ČD. Ń¹Ēæ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com