
| A. | 若D是白色沉淀,D与A的摩尔质量相等,则X可能是铝盐 | |
| B. | 若X是Na2SO3,C是气体,则A可能是氯气,且D和E能发生反应 | |
| C. | 若D是CO,C能和E反应,则A是Na2O2,X的同素异形体只有3种 | |
| D. | 若A是单质,B和D的反应是,则E一定能还原Fe2O3 |
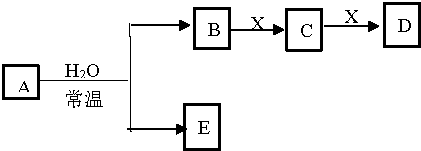
分析 A、D为白色沉淀,可以判断为OH-与Al 铝离子生成偏铝酸根,偏铝酸根离子再与铝离子生成Al(OH)3,X为铝盐,C为偏铝酸盐,铝盐和偏铝酸盐在溶液中发生双水解反应生成Al(OH)3.
B、若X是Na2SO3,则A可能是氯气,则B为HCl,E为HClO,C为气体SO2,D为NaHSO3,D和E能发生氧化还原反应.
C、D为CO,可以判断O2 $\stackrel{C}{→}$CO2$\stackrel{C}{→}$CO,X为C,B为O2,C为CO2,A与水反应生成氧气,A为过氧化钠或氟气,结合二氧化碳能与E反应判断;
D、根据B、D反应的离子方程式OH-+HCO3-═H2O+CO32-,A为活泼金属Na,B为NaOH、E为H2,X为CO2,C为Na2CO3,D为NaHCO3.
解答 解:A、D为摩尔质量为78g/mol的Al(OH)3,A为摩尔质量为78g/mol 的Na2O2,X为铝盐,C为偏铝酸盐,铝盐和偏铝酸盐在溶液中发生双水解反应生成Al(OH)3,符合转化关系,故A正确;
B、若X是Na2SO3,则A可能是氯气,则B为HCl,E为HClO,C为气体SO2,D为NaHSO3,D和E能发生氧化还原反应,符合转化关系,故B正确;
C、如A为氟气,HF与二氧化碳不反应,A为Na2O2,B为O2,E为NaOH,X为C,C为CO2,D为CO,符合转化关系,碳的同素异形体有金刚石、石墨、无定形碳、足球碳等多种,故C错误;
D、根据B、D反应的离子方程式OH-+HCO3-═H2O+CO32-,A为活泼金属Na,B为NaOH、E为H2,X为CO2,C为Na2CO3,D为NaHCO3,H2在加热时能还原Fe2O3,故D正确;
故选C.
点评 本题考查元素及其化合物的转化关系,题目难度中等,做好本题的关键之处在于把握好物质的性质,解题关键是转化关系的分析判断.


科目:高中化学 来源: 题型:选择题
| A. | 硫酸钠晶体溶于水中 | |
| B. | NH4HCO3(s)分解生成NH3(g)、CO2(g)和H2O(g) | |
| C. | 水结成冰 | |
| D. | 干冰升华 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | M层上有2对成对电子 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
| J | J的气态氢化物与J的最高价氧化物对应的水化物可反应生成一种盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌片溶解了1mol,铜片上析出1mol氢气 | |
| B. | 两极上溶解和析出的物质的质量相等 | |
| C. | 锌片溶解了1g,铜片上析出1g氢气 | |
| D. | 电解质溶液pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油的炼制过程都是化学变化 | |
| B. | 煤干馏的液态产物主要有煤焦油、粗氨水 | |
| C. | 石油裂解是为了提高汽油等轻质油的产量 | |
| D. | 煤的液化是物理变化,煤的气化是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用NaOH溶液吸收Cl2制备消毒液:Cl2+2OH-→Cl-+ClO-+H2O | |
| B. | 该消毒液与洁厕灵混用会引起中毒:2H++Cl-+ClO-→Cl2↑+H2O | |
| C. | 常温下,该消毒液的pH≈12是因为:ClO-+H2O?HClO+OH- | |
| D. | 该消毒液加少量白醋可增强消毒能力:CH3COOH+ClO-→HClO+CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 6mol | B. | 4.7mol | C. | 3mol | D. | 2.4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种无毒的气体均为还原产物 | |
| B. | 反应后溶液的pH会升高 | |
| C. | 氧化剂与还原剂的物质的量之比为5:2 | |
| D. | 每转移2NA个电子时,一定会生成13.44 L的气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com