
| A. | Na2CO3的溶解性比NaHCO3小 | |
| B. | SiO2与酸、碱均能反应,属于两性氧化物 | |
| C. | FeCl3溶液制作铜质印刷线路板的离子反应为2Fe3++Cu═2Fe2++Cu2+ | |
| D. | Fe在足量Cl2中燃烧生成FeCl2和FeCl3 |
分析 A.相同条件下,碳酸钠的溶解性大于碳酸氢钠的;
B.与酸或碱反应生成盐和水的氧化物,为两性氧化物;
C.氯化铁和铜反应 生成氯化亚铁和氯化铜;
D.Fe在足量Cl2中燃烧只生成FeCl3.
解答 解:A.饱和Na2CO3溶液中通入过量二氧化碳气体可得到NaHCO3沉淀,说明Na2CO3比NaHCO3易溶于水,故A错误;
B.与酸或碱反应生成盐和水的氧化物,为两性氧化物,而二氧化硅与盐酸、硫酸等不反应,只属于酸性氧化物,故B错误;
C.氯化铁和铜反应生成氯化亚铁和氯化铜,离子反应为2Fe3++Cu═2Fe2++Cu2+,所以FeCl3溶液可用于铜质印刷线路板制作,故C正确;
D.因为氯气具有强氧化性,则Fe在足量Cl2中燃烧只生成FeCl3,故D错误;
故选C.
点评 本题主要考查了元素化合物的知识,考查角度广,要求学生具有分析和解决问题的能力,平时注意相关知识的积累,题目难度中等.


科目:高中化学 来源: 题型:解答题
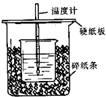 测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.
测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.| 温度 实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | 4.0 |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(A)增大时,v增大,k也增大 | B. | c(B)增大时,v增大,k值不变 | ||
| C. | 升高温度时,v增大,k值不变 | D. | 升高温度时,v值不变,k增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知NH3和HCl都能用来作喷泉实验的气体,若在相同条件下用等体积烧瓶各收集满NH3和HCl气体,进行实验(两烧瓶内充满溶液且不考虑溶质的扩散).下列说法错误的是( )
已知NH3和HCl都能用来作喷泉实验的气体,若在相同条件下用等体积烧瓶各收集满NH3和HCl气体,进行实验(两烧瓶内充满溶液且不考虑溶质的扩散).下列说法错误的是( )| A. | NH3和HCl分别形成蓝色、红色喷泉 | |
| B. | 制备干燥的NH3和HCl,所需的干燥剂分别是碱石灰、浓硫酸 | |
| C. | 改为NO2气体,所得溶液溶质的物质的量浓度与前两者不同 | |
| D. | 去掉装置中的胶头滴管,改为单孔塞,也可引发喷泉 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有① | B. | ①② | C. | ②③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100 mL 2 mol•L-1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 | |
| B. | 将相同大小、形状的铝条与稀硫酸和浓硫酸反应时,稀硫酸产生氢气快 | |
| C. | 将氢气和氯气的混合气体分别放在冷暗处和强光照射下,会发现光照下有氯化氢生成 | |
| D. | 两支试管中分别加入相同浓度相同体积的双氧水,其中一支试管再加入少量二氧化锰,产生氧气的快慢不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤⑥ | B. | ①③⑤⑥ | C. | ①④⑤ | D. | ②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com