
A、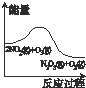 升高温度,NO2的含量减小 |
B、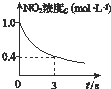 0~3 s内,反应速率为v(NO2)=0.2 mol?L-1 |
C、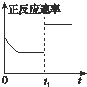 t1时仅加入催化剂,平衡正向移动 |
D、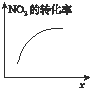 达平衡时,仅改变x,则x可能为压强 |
| △c |
| △t |
| 0.6mol/L |
| 3s |


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:
A、 实验室中浓硝酸应保存在棕色细口瓶中,并贴有如图所示标签 |
| B、制备Fe(OH)3胶体时,应向沸水中逐滴加入1mol?L-1的FeCl3溶液,并继续加热到液体呈透明的红褐色为止 |
| C、用托盘天平称取5.85g NaCl,称量时砝码放在右盘,氯化钠放在左盘 |
| D、用50mL量筒量取5.6mL浓硫酸 |
| E、用四氯化碳萃取碘水中的碘,分液时有机层从分液漏斗的下端放出 |
| F、用广泛pH试纸测得某溶液的pH为4.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、I2 |
| B、KI |
| C、KIO3 |
| D、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2SO4 的摩尔质量是 98 g |
| B、1 mol H2O的质量是 18 g/mol |
| C、Cl-的摩尔质量是 35.5 g/mol |
| D、1 mol H2O中含有2 mol H和1 mol O |
查看答案和解析>>
科目:高中化学 来源: 题型:
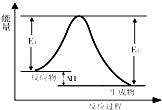 关于反应3A (g)+B (g)?2C (g) 发生过程中的能量变化如图,下列说法中不正确的是( )
关于反应3A (g)+B (g)?2C (g) 发生过程中的能量变化如图,下列说法中不正确的是( )| A、该反应为放热反应 |
| B、反应体系中加入催化剂,E1、E2减小,△H不变 |
| C、增大反应体系压强,化学平衡正向移动,气体B的浓度减少 |
| D、降低反应体系温度,反应速率减慢,A的转化率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
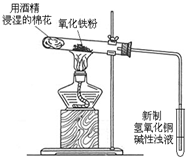 某课外小组同学做了如下探究实验:将蘸有饱和氯化铁溶液的粉笔,用坩埚钳夹持置于酒精灯火焰上灼烧,一分钟内可观察到如下颜色变化:黄色(氯化铁溶液)--红褐色(A)--铁锈红色(B)--黑色(C).
某课外小组同学做了如下探究实验:将蘸有饱和氯化铁溶液的粉笔,用坩埚钳夹持置于酒精灯火焰上灼烧,一分钟内可观察到如下颜色变化:黄色(氯化铁溶液)--红褐色(A)--铁锈红色(B)--黑色(C).查看答案和解析>>
科目:高中化学 来源: 题型:
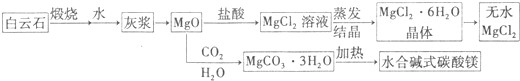
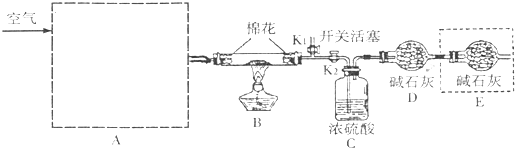
查看答案和解析>>
科目:高中化学 来源: 题型:
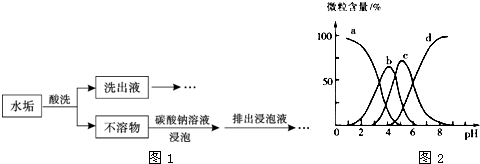
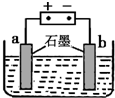
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com