
 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:选择题
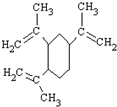
| A. | 榄香烯的分子式为C15H20 | |
| B. | 榄香烯属于芳香烃 | |
| C. | 1 mol 榄香烯最多能和3 mol H2反应 | |
| D. | 榄香烯不能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 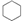 和CH2CH-CH2CH2CH2CH3 和CH2CH-CH2CH2CH2CH3 | B. | 正戊烷和新戊烷 | ||
| C. | CH3-O-CH3和CH3CH2OH | D. | 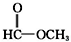 和 和 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | XY2 | B. | X2Y3 | C. | X3Y2 | D. | X2Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
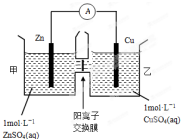 化学与人类生产和生活中密切相关,掌握有关的化学基础知识可以改善我们的生活.
化学与人类生产和生活中密切相关,掌握有关的化学基础知识可以改善我们的生活.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都具有强氧化性 | |
| B. | 在常温下都能与铜反应 | |
| C. | 露置于空气中都能形成白雾 | |
| D. | 在空气中长期露置,溶液质量均减轻 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com