
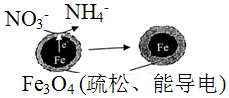
| A. | 能量转化形式主要为化学能转化为电能 | |
| B. | 电极材料分别为Fe和Fe3O4 | |
| C. | 负极反应为:NO3-+8e-+l0H+═NH4++3H2O | |
| D. | 该原理的总反应可表示为:NO3-+3Fe+2H++H2O═NH4++Fe3O4 |
分析 构成的原电池中,Fe失电子作负极,生成亚铁离子,NO3-在正极上得电子生成NH4+,结合原电池原理分析.
解答 解:A.该装置构成了原电池,原电池中化学能转化为电能,故A正确;
B.Fe失电子作负极,Fe3O4作正极,故B正确;
C.Fe失电子作负极,生成亚铁离子,NO3-在正极上得电子生成NH4+,则正极反应为:NO3-+8e-+l0H+═NH4++3H2O,故C错误;
D.反应原理是铁与硝酸根离子反应生成四氧化三铁和铵根离子,即该原理的总反应可表示为:NO3-+3Fe+2H++H2O═NH4++Fe3O4,故D正确.
故选C.
点评 本题考查了原电池原理的应用,注意根据得失电子来判断正负极上发生的反应,明确正负极上发生的反应是解题的关键,题目难度中等,侧重于考查学生的分析能力和应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)=2H2O(g)△H 1; 2H2(g)+O2(g)=2H2O(l)△H2 | |
| B. | S(s)+O2(g)=SO2(g)△H 1; S(g)+O2(g)=SO2(g)△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)=CO(g)△H 1; C(s)+O2(g)=CO2(g)△H2 | |
| D. | H2(g)+Cl2(g)=2HCl(g)△H 1; $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)=HCl(g)△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{灼烧}{→}$MgO$\stackrel{电解}{→}$Mg | |
| B. | 由NaCl制漂白剂:NaCl(aq)$\stackrel{电解}{→}$Cl2$\stackrel{石灰乳}{→}$漂白粉 | |
| C. | 由铝土矿冶炼铝:铝土矿$→_{Na_{3}AlF_{6}}^{电解}$Al | |
| D. | 合成NH3:NH4Cl和Ca(OH)2固体$\stackrel{△}{→}$NH3$\stackrel{碱石灰}{→}$纯净干燥的氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O、CaO、Al2O3均为碱性氧化物 | |
| B. | 水玻璃、漂白液、液氯均为混合物 | |
| C. | 氨水能够导电,所以氨水是电解质 | |
| D. | 有单质参加或生成的化学反应不一定是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 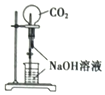 喷泉实验 | B. |  配制一定物质的量浓度的NaCl溶液 | ||
| C. | 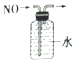 排水法收集NO | D. |  碳酸氢钠受热分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
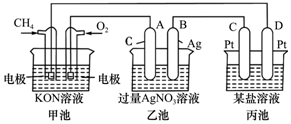 根据下列电化学装置,回答下列问题:
根据下列电化学装置,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO的摩尔质量为30g | |
| B. | 常温常压下,14g一氧化碳所占体积为11.2 L | |
| C. | 等物质的量的Na2O2和Na2O中所含阴阳离子总数相等 | |
| D. | 设阿伏加德罗常数为NA,常温常压下O2与O3的混合物32g,含有分子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com