
| 编号 | 气体 | a | b | c | 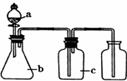 |
| A | NH3 | 浓氨水 | 生石灰 | 碱石灰 | |
| B | CO2 | 盐酸 | 碳酸钙 | 饱和NaHCO3溶液 | |
| C | NO | 稀硝酸 | 铜屑 | H2O | |
| D | Cl2 | 浓盐酸 | 二氧化锰 | 饱和NaCl溶液 |
| A. | A | B. | B | C. | C | D. | D |
分析 由题给装置可知不加热条件下制备气体,c为净化装置,用向上排空气法收集气体,说明气体的密度比空气大,以此解答该题.
解答 解:A.氨气密度比空气小,应用向下排空法收集,且c一般用于盛装液体干燥剂,碱石灰应放在干燥管中,故A错误;
B.盐酸和大理石反应制取二氧化碳不需加热,二氧化碳中混有易挥发的氯化氢,二氧化碳与碳酸氢钠不反应,氯化氢与碳酸氢钠反应生成氯化钠和二氧化碳和水,能用碳酸氢钠进行洗涤二氧化碳,二氧化碳密度比空气大,能用向上排空气法收集,故B正确;
C.铜和稀硝酸反应生成一氧化氮不需要加热,但一氧化氮难溶于水,所以不能用水洗,一氧化氮和氧气反应生成二氧化氮,所以不能用排空气法收集,故C错误;
D.浓盐酸和二氧化锰的反应应在加热条件下进行,故D错误.
故选B.
点评 本题考查了气体的制备、净化、收集装置的选择,为高频考点,侧重于学生的分析、评价能力的考查,注意把握气体的收集方法时要考虑气体的密度、溶解性、稳定性,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 气态氢化物的稳定性:Y<M | |
| B. | 简单离子半径由大到小的顺序是:M>Y>Z | |
| C. | 化合物Z2Y2 中含有离子键和非极性共价键 | |
| D. | 等浓度的X2M与Z2M的溶液中,水的电离程度:X2M<Z2M |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
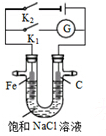
| A. | K1闭合,石墨棒上发生的反应为2H++2e→H2↑ | |
| B. | K2闭合,铁棒不会被腐蚀,属于外加电流的阴极保护法 | |
| C. | K2闭合,石墨棒周围溶液pH逐渐升高 | |
| D. | K1闭合,电路中通过0.004NA个电子时,石墨棒上产生0.001mol气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
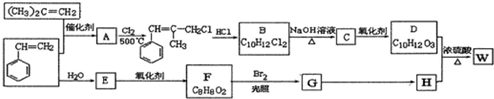
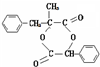 .
.  ;由D生成高分子化合物的方程式为
;由D生成高分子化合物的方程式为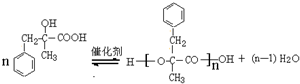 .
.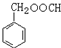 (写结构简式).
(写结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
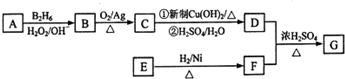
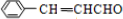 .
.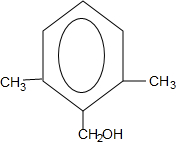 或
或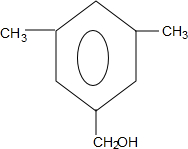 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径的大小顺序:r(B)>r(C)>r(D) | |
| B. | B的简单气态氢化物的热稳定性比D的弱 | |
| C. | E分别与A、C形成的化合物中化学键类型相同 | |
| D. | C的最高价氧化物对应水化物的碱性在同周期中最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


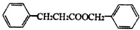 ;有机物M中含氧官能团名称是醛基.
;有机物M中含氧官能团名称是醛基.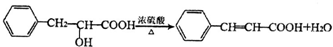 ,F→G
,F→G .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com